�i�P�j�@�ÌŁ@
�@
�i�P�|�P�j�@�j�����Ɛ���
�@�Ìł͉t�̂���ő̂ւ̑��ϑԂł���A�t�̖̂������ȍ\���̂Ȃ����牷�x�ቺ�ɂ�茋���̊j�ƂȂ�
�אڌ��q�̔z�u�������ɋ߂����q�z�u���G���u���I���������A���̂Ȃ�������R�ՊE���a���傫�����̂�
�`�������ƈ���ƂȂ萬������B
�@�@
 �@�@
�@�@�@�@�@�@�ЁF�\�ʃG�l���M�[�A���f���F�ϑԂ̋쓮���R�G�l���M�[�A�s���F�Z�_�A�g���F���M�A���s�F�ߗ�x
�@�ՊE���a�͉ߗ�x�ƂƂ��ɏ������Ȃ�B�j�����͕\�ʃG�l���M�[���傫���e������B
�@�j�����ɂ͎��͂̉e�����Ȃ��ώ��j�����ƚ��ĕǖʁA�s�������q���̉e������s�ώ��j����������B
�@�ʏ�̋����̋Ìłł͊j�����̐���͂ł��Ȃ����瑽�����ƂȂ�A�e�����͌������E�Őڂ��邱�ƂƂȂ�B
�@�����������K�肷��̂͌ʼnt�E�ʌ`��ƗD�搬�����ʂł���B
���ʼnt�E�ʌ`��
�@�ʼnt�E�ʌ`��͔M�E�����ړ�����ѐ��M�ƊE�ʃG�l���M�[�ɂ���ċK�肳���B
�@�ʼnt�E�ʂ͌ő̂���t�̂�ʂ��ĉ��x�������Ȃ鐳�̉��x���z�ŕ����ƂȂ�A����t�̂ʼn��x���ቺ����
���̉��x���z�ł͌ʼnt�E�ʂ����ꌋ���g�D�ɉe�����ł�B
�@
�@����ȊE�ʂ������ƂƂ��ɕs����ɂȂ錻�ۂ�Mullins-Sekerka�s�����������B
�@����ȊE�ʂ͐������x�ƂƂ��ɃZ����cellular�A����columnar�f���h���C�g�A����equiaxed�f���h���C�g�ƕω�����B
�@

���ÌŎ��̑g���ω���
�@���t��Ԃ̋Ìłł͉t���͉t�����ɉ����āA�ő��͌ő����ɉ����đg���ω����A�ő��Ɖt���̊�����
�Ă��̌����ɏ]���B
�@�s�����Z�x��Scheil�̎��ɏ]���Ƃ����B�i�t���Z�x��l�Ōő��ł̊g�U���Ȃ��Ƃ�������j
�@�@�@�@�@�b�������b�O�i�P�|�����j���|�P�@k�F���z�W���@�����b���^�b�k�A�����F�Ìŗ�
�@���������ۂɋÌł͔t��ԂŐi�ݗn�����f�͉t���ɔZ�k����A�ő��A�t���Ƃ��ɓ����ɔZ�x���z��������B
�@�t�����ł͊g�U�ƑΗ��������A�ő��ł͊g�U��������B
���g���I�ߗ�constitutional undercooling��
�@�����n�ł͗n���̕ΐ͂̂��߉t�����̎��ۂ̉��x���z���Z�x���z�ɑΉ��������z�̉��x���z���Ⴂ
�i�g���I�ߗ��j���Ƃ�����A���̂��ߕ����E�ʂ��s���艻����B
�@�g���I�ߗ�͋ÌŎ��ɂ͑��݂����Ìł̐i�s�ʼnߗ�i�Z�_��������j��������B
��Gibbs-Thomson���ʁ�
�@�ʼnt�E�ʂ��ʌ`��i�ȗ����j�ɂȂ�ƁA�t�̒��̌ő̂̎��R�G�l���M�[�͋Ȗʂɂ��������͏㏸�ɂ�肻�̌a��
����Ⴕ�đ����A
�@�@�@
�@�@�@�@�FGibbs-Thomson�W���A�j�F�ȗ��A�ЁF�E�ʃG�l���M�[�A�s�l�F�Z�_�A���g�Z���G���^���s�[�A�ρF�ȗ����a
�Ȃ�ߗ�p���s�q�i�ȗ��ߗ�j��������B�i���Ȃ킿�ȗ����ɂȂ�ƗZ�_�������邱�ƂɂȂ�B�j�����Gibbs-Thomson�����Ƃ����B
�@
�@�M�g�U�ɂ����M�̏����ƊE�ʌ`��ɂ��Gibbs-Thomson���ʂ�Mullins-Sekerka�s����̊�{�I�d�g�݂ł���B
�@�����ʕ����`�������ƔM�����o����₷���Ȃ萬������������邪�AGibbs-Thomson���ʂŗn���₷���Ȃ�}���ɓ����B
�����}�f���h���C�g�@dendrite��
�@������������萬��������ƌ����ɓ��L�̊O�`�i���ւ��j�Ő������邪�ʏ�̌��������ł͎��}�ƂȂ�B
�@���}�͉ߗ�p��Ԃɂ���n�t����̋ÌłɌ����錋�������̈�`�Ԃł���B
�@�����͎��}��Ɏ}�����ꂵ�Ȃ���}���x�ŋN����A�e�}�̕����͐��m�Ɍ����w�I�ɓ���̕����Ɉ�v����B
�@�ʼnt�E�ʂ������ƕ����Ȗʂ���Z����i�ȗ����������ˋN��j�X�Ɏ��}��ƂȂ�B
�@�ʼnt�����͈͂��L���Ìŋ�Ԃ��L���ꍇ�����}�ɂȂ�₷���B
�����������̋쓮�͂ƂȂ�ߗ�x���s�͔M�I�ߗ�x���s���A�g���I�ߗ�x���s���AGibbs-Thomson���ʂɂ��ȗ��ߗ�x
���s�q�A�E�ʋ쓮�͂ł��铮�I�ߗ�x���s������Ȃ�B
�@�@�@���s�����s���{���s���{���s�q�{���s��
�@�M�I�ߗ�x�͔M�`���������������ē�����Ivantsov���h���i�oe�j�ɂ���ė^������B
�@�@�@�i�oe�����u�^�Q�c���y�N�����ƌĂ�A���F���a�A�u�F�������x�A�c�F�g�U���j
�@�@�@���s�������g�~�h���i�o�j�^�b�@�@�b�F�̐ϔ�M�A���g�F�̐ϓ���Z���G���^���s�[
�@���I�ߗ�x���s���͎����ŗ^������B
�@�@�@
 �@�u�F�������x�A���O�F���`���͊w�W��
�@�u�F�������x�A���O�F���`���͊w�W���i�P�|�Q�j�@�����̊O�`
�@���������ɂ͊O���̈Ⴂ�����t�@�Z�b�gfaceted�������m���t�@�Z�b�gnon faceted����������B
�@

�@�E�t�@�Z�b�gfaceted����
�@�@�����O�`������̌����ʂ���Ȃ镽��Ȗʁi�t�@�Z�b�g�j�ň͂܂ꂽ�`�Ԃ������B
�@�@���ʐ����@�\�ɂ��B
�@�E�m���t�@�Z�b�gnon faceted����
�@�@�����O�`�͓���̌����ʂ���Ȃ镽��Ȗʂ������Ȃ����A��́i���j��}�i�r�j�̕����͌����w�I�ɓ���̕����Ɉ�v����B
�@�@�A�������@�\�ɂ��B
�@�@
�i�P�|�R�j�@�����̐����@�\
�i�P�|�R�|�P�j�@���ʐ����ƘA������
�@�t�@�Z�b�g�����ƃm���t�@�Z�b�g�����͂��ꂼ�ꉈ�ʐ����ƘA�������@�\�ɂ��B
������lateral�������@�i�w�����Astepwise�����A edgewise�����j
�@�@�@�E�ʂ͌��q�I�ɕ��R�Łi���R�Ȗʂ��e���X�Ƃ����j�A���q�̓G�b�W�i�X�e�b�v�A�i�j��W���O�i�L���N�A�X�e�b�v�̊p�j�ɕt�����A������
�@�@����ȃG�b�W�ʁi���Ȗʁj�������B
�@�@�@�����̋쓮�͂��������A���t�ɋ߂����������ŋN����B
�@�@�@�t�@�Z�b�g�����������B��ɔ�����B
�@�@�@�X�e�b�v�̋����̎d���ɂ��Q�����i�\�ʁj�j���������ƉQ��������������B
�@�@�E�Q�����i�\�ʁj�j��������
�@�@�@�@����Ɍ��������j���`�������B
�@�@�@�@�������x�u��exp�i�|�P�^���ʁj�@�@�i���ʁF�쓮�́A�ő��Ɖt���̉��w�G�l���M�[���j
�@�@�E�Q����spiral����
�@�@�@�@�点��screw�]�ʂɂ��X�e�b�v�����������B
�@�@�@�@�������x�u��i���ʁj�Q�@�@
���A���������@�i����normal�����A�t�������j
�@�@�@���q�I�ɍr�ꂽ�ʁA�g�U�E�ʁA���q�͊E�ʂɋψ�ɕt���A�}�N���I�ɂ͕��R�œ���ȃG�b�W��ʂ��Ȃ��B
�@�@�@�m���t�@�Z�b�g�����������A��ɋ����B
�@�@�@�ߖO�a�x�̑傫�ȋC�������ȂǂŋN����B
�@�@�@�r�ꂽ�ʂȂ̂ŃX�e�b�v�A�L���N�͑������݂���B
�@�@�@�������x�u�僢��
�@

�@�E���t�j���O�]��
�@�@�K���I�ɔz�����R�Ȗʂ������\�����疳�����ȍr�ꂽ�ʂ������\���ւ̕ω������t�j���O�]�ڂƂ����B
�i�P�|�R�|�Q�j�@Jackson���f����Cahn���f��
�@�r�ꂽ�ʂƕ��R�Ȗʂ̐������f���Ƃ���Jackson���f����Cahn���f��������B
�@
�@�EJackson���f��
�@�@�@���R�Ȗʂ��e���ʂ��͕����̓����Ɩʂ̌����w�I�����ɂ��B
�@�@Jackson�̍r���p�����[�^�[��
�@�@�@�@�@�@�����̃��r�^�q�@�@�@�@�@���r�����g�^�s�@�@���r�F�n�Z�G���g���s�[�A���g�F�n��M
�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�́F�����w���q�����P
�@�@�@�����Q�@�@�@�@�@�@�@�@�@�A�������A�m���t�@�Z�b�g�����@�r�ꂽ��
�@�@�@�����Q�@�@���ʐ����A�t�@�Z�b�g�����@���R�Ȗ�
�@�ECahn���f��
�@�@�@���ʐ�������A�������ւ̕ω��͊E�ʂ̉ߗ�p����ɂ��B
�@�@�@�A�������͉ߗ�p����A���ʐ����͉ߗ�p�����B
�@�@�@�����͒�ߗ�p�ł��A���������N����B
�@�@�@��ߗ�p����h�点���A�Q�����j�����A�A�������h�ƕω��B
�@�@�@�@�@
�i�P�|�R�|�R�j�@�x���O���ʁi���ہj
�@���������ł͑��ʑ̌����̕���Ȗʂ͗ł�����ߖO�a�x���������Ȃ�A�]���ėł���̌����������x���傫���Ȃ�B
�@���̌��ʂ������Ȃ�ƌ����̗ł�����o������A����Ȗʂ��������[���������A�X�Ɏ��}�A���ƕω�
����B
�@�ߗ�p�x���������ƌ����̓t�@�Z�b�g�i���`�j���Ƃ邪�A�傫���Ȃ�Ə��Ɋ[���A���}�A���ƂȂ�X�ɂ̓K���X������B
�����ȂƏ���
�@����habitus
�@�@�����ʂ̔��B�̒��x�̈Ⴂ�Ő����錋���`�Ԃ̈Ⴂ�A�l�p���A�l�p���E�E�E
�@�@�������̂̐������x�ٕ̈������邢�͊������ٕ̈����ɂ���Đ�����B
�@����tracht
�@�@�ʂ̑g�ݍ��킹�Ɣ��B�̒��x�̕ω��ɂ���Ă����錋���̌`�ԕω��A���U�ʑ́A���W�ʑ́A�E�E
�@�@�����ʂ̐������x�̊������i���x�A�ߖO�a�x�A�n�}�A�s�����E�E�j�̈ˑ����ɂ���Đ�����B
�i�Q�j�@�ΐ́i�Ìŕΐ́j�@�@
�@�������f��s�����Ȃǂ̗n�����f���ܗL���Ă���n�Z�������Ìł��鎞�́C�n�����f�͕ΐ͂���B
�@���f�̕ΐ͂ɂ̓~�N���ΐ͂ƃ}�N���ΐ͂Ƃ�����B�@
�@�ΐ́i�Ìŕΐ́j��������̂͗n�����f�̌ő��Ɖt���ւ̔z�����������z�W�������P�łȂ����ƂɋN������B
�@�܂������̌ő����Ɖt�����̉��x�͈́i�ʼnt�����͈́j���L�����Ƃɂ��N������B
�i�Q�|�P�j�~�N���ΐ́@�@
�@�n�����f�̗n��x�́A�t�̒��ɔ�ő����̕����Ⴂ�B���������āA�Ìł̐i�s�ɂƂ��Ȃ��t�̒��ɁA
�n�����f���r�o����Z������B
�@���̂��߃f���h���C�g�Ìłł͎厲�̐�������ё��}�̔��B�ɔ����ʼnt�Ԃ̗n�����f�̕��z���A���
�Ìł����f���h���C�g�̕����͗n�����f�i�������f�j�̔Z�x�����Ȃ��A��ŋÌł���f���h���C�g�̕����ƂŔZ�x�����i�����ΐ́j�A
�܂��f���h���C�g�Ԃ܂�Ìŗ��E�ɂ́A�n�����f��s�������Z�k�����B�i���E�ΐ́j
�i�Q�|�Q�j�@�}�N���ΐ́@
�@�}�N���ΐ͂Ƃ́C�f���h���C�g�Ԋu�⌋�����Ԋu�����������ɂ킽�����I�Ȏړx�ł݂���ΐ͂������B
�@�}�N���ΐ͂́C��ʂɃ~�N���ΐ͂ɂ���ĔZ�����ꂽ�t�����������邽�߂ɋN����̂��قƂ�ǂł���A
���x������єZ�x���ɋN�����鎩�R�Η��C�\�ʒ��͗��C�d���͂�ÌŎ��k�͂Ȃǂɂ���ė�������B
�@�Ìł͒��^�ɐڐG�����O����������ɐi�ނ����Z�_������s�����͒��S���ɕΐ͂���B
�@���̂悤�ɋÌł̒x�������ɕs���������ΐ͂���ꍇ������ΐ��Ƃ����B
�@�`����������ȂǂŊO���i�\�ʂȂ����Ìł̑��������j�ɕs���������ΐ͂���ꍇ���t�ΐ��Ƃ����B
�@����͋ÌŁE��p�ɂ����k�Ō^�Ƃ̊Ԃɋ������A���̌��ʕ��M�������Ȃ�A�M�`�����̂����`������
��b�������ł͋Ìŕ��̍ėn�Z���N���邽�߂Ƃ����B
�@
�@�܂��O�q�̂悤�ɗn�����f�̗n��x�́A�t�̒��ɔ�ő����̕����Ⴂ�B���������āA�Ìł̐i�s�ɂƂ��Ȃ��t�̒��ɁA
�n�����f���r�o����A�x���ɋÌł��������ɔZ�����A���ϑg�����Z�x�̍������ΐ����N�����A����A���ϑg�����Z�x��
�Ⴂ�ꍇ�����ΐ��Ƃ����B
�@�A�������ł͒��S�ΐ͂�����邽�߂ɍs���d�����a�ɂ��~�N���ΐ͂����n�����f���o���ꂽ��A�����ƈړ��i�����j��
��蒆�S���̖��Ìł̉t�����i�肾���ꂽ�肷�邱�Ƃɂ�荇���|�Ȃǂł̂b���A�m���A�b�Ȃǂ̕��ΐ͂�������B
���ΐ͈͂ȉ��̂悤�ɕ��ނł���
�@�@�Ìŕΐ�
�@�@�@�@�}�N���ΐ́@�E�E�E����x��
�@�@�@�@�~�N���ΐ́@�E�E�E�ʂ��I�[�_�[
�@�@�@�@�@�@�����ΐ́i�����ΐ́j�@�@�E�E�E�����̒��S�Ǝ��ӁA�f���h���C�g�̎�}�Ƒ��}�̊ԁA�n�����f�̌ő��ł̊g�U�̂��ɂ����ɂ��B
�@�@�@�@�@�@�i�Ìłɂ��j���E�ΐ�
�@�i�Ìłɂ��Ȃ��j���E�ΐ́@�E�E�E�����I�[�_�[�@�@�@����q
�@�@�@�@���t�ΐ�
�@�@�@�@�t�ΐ�
�����J���b�Z���Xrecalescence�i�ċP���ہj
�@�ߗ�x���傫���Ȃ�ƁA�Ìłɔ����������ώ@���ꂱ������J���b�Z���X�Ƃ����B
�@�ÌŎ��̐��M�̉���Ő��������B
�@�ߗ�p��傫�����Ă����ƋÌŐ��M�̕��o�ɂ�莎���̉��x���}�ɏ㏸���镜�M���ۂ�������B�@
�@�i�ʏ�̋Ìłł͋Ìł��I���܂Ő��M�ʼn��x����ԂɂȂ�j
�@���E��E���Ȃǂ̋������A�Z�_�����ɂ��ď����E�~�����J��Ԃ��ƍő�ߗ�x�͖�200���ɒB����B�@
�@���V�@�ɂ�閳�e��Ìłł��傫�ȉߗ�x������ꃌ�J���b�Z���X��������B
�i�R�j�@��������i�C���S�b�g�j�@
�@���^�����ɂ�钒��͋��^�ɐڂ��镔���͋}��Ƒ����̊j�����ɂ����ɏ����ȓ��������`������
�i�`���w�j�A���̂Ȃ��̗D�搬��������L���錋�����D�搬�����Ē����`�������B
�@�����ɂ͕������������Ȃ����������`�������B
�@
�@���Y�������コ���邽�ߌ��݂͘A�����������S�ł��邪�A�������ł͕\�ʂ��Ìł��A�Ȃ������Ìł̏�Ԃ�
�������s����B
���S�|�̑���
�@�|�̋Ìłł͗n���_�f�̏��������ɏd�v�ŗn���_�f�̓V���R���i�e���r���t�F���V���R���j�A�A���~�j�E���A�}���K���i�e���l��
�t�F���}���K���j�Ȃǂɂ���ď����i�E�_�A�_�������������j����A�E�_���s��Ȃ��Ǝ_�f���b�ƌ�������������ɂb�n����
�n���͕������i���~���O�E�A�N�V�����j�A�ŏ��̋Ìł����\�ʂɋC�A����B
�@�|�͒E�_�̒��x�ŃL���h�|�A�Z�~�E�L���h�|�A�L���b�v�h�|�A�����h�|�ɕ�������B
�@�L���h�|
�@�@���������i�ÌŁj�̍ہA�\���E�_���s���i�V���R����A���~�j�E�����̓Y���j�A�K�X�i�b�n�j���o�̂Ȃ��Â��ȏ�Ԃ�
�@�Ìł������|�B
�@�@�C�A���Ȃ��g�D���قڋψ�ŕΐ͂̏��Ȃ��D�ꂽ�����������㕔�Ɉ������i���k�E�j�����������܂肪�����B
�@�@�����|�⍇���|�B
�@�Z�~�E�L���h�|
�@�@�����h�|�ƃL���h�|�̒��Ԃ̒E�_���s�������̂ŏ]���Đ��������̒��ԂƂȂ�B
�@�L���b�v�h�|
�@�@�n�|�𒒌^�ɒ�������̎��Ԃ��o�߂��Ă���`���𓊓�����i�P�~�J���L���b�v�h�|�j���A���邢�͒��^�ɊW������
�@�i���J�j�J���L���b�v�h�|�j���~���O�����𑁂߂ɋ����I������������Â��ɋÌł������|�B
�@�@���̂悤�ɂ��ĕ\�w���������h�|�̂悤�Ȑ���Ȃ��̂Ƃ���ƂƂ��ɁA�������Z�~�L���h�|�̂悤�ȕΐ͂̏��Ȃ���ԂƂ��A���C�A
�@�ɂ���Ď��k�E�E���悤�Ƃ������́B
�@�����h�|
�@�@�@�t�F���}���K���Ōy���E�_������x�ŁA�]���ăK�X����o�E�����i���~�C���O�����j���Ȃ���Ìł��邽�ߍŏ��ɋÌł���
�@�@�\�ʂɋC�A���܂މ��w�i�����w�j��������B
�@�@�@�����ł͓����̋C�A���Ԃ�ǍD�ł��邪�؍킷��Ɠ����̏����I�o����̂őY�����H�����Ő؍���H�ɂ͌����Ȃ��B
�@�A������
�@�@�A�������ł͗n�|�𑤖ʂ��Ìł�����ԂŒ��^�̒ꂩ������o���Ă����������s���B���̂��߂ɂ͗n�|�̕s�������ł��邾��
�@��������ƂƂ��ɁA�Ō�ɋÌł��钆�S���ւ̕s�����ΐ͂�h���K�v������B
�@�@�ʏ�`���L���h�|�ł���B
�i�S�j�@���������̋Ì�
�i�S�|�P�j�@���������̓����I�Ìőg�D
�@���������n�ł͑����t�̗l���i��Ԑ}����킩��j��������I�ȑg�D��悷����̂�������B
�@�E����eutectic�g�D
�@�@�����͉t�������̌ő��������ɋÌł��锽���ł���B
�@�@�@L�i�t���j�����i�ő��j�{���i�ő��j�@
�@�@�����͂Q���̑̐ϔ�őw��g�D�A�_��g�D�Ȃǂ������B
�@�@��Z�_�����߂���͂͋�������{�Ƃ���B
�@�@�@�w��g�D�@
�@�@�@�@�Q���̑̐ς��߂��ꍇ�AAl-Cu�APb-Sn�ȂǂɌ�����B�@
�@�@�@�_��g�D�@�@
�@�@�@�@�Q���̑̐ςɍ�������ꍇ�B
�@�@

�@�E�Ώ�monotectic�g�D�@
�@�@�Ώ��͉t������ő��Ɖt�����������锽����
�@�@�@�@L��L�f�{��
�@�@�c�����t�����₪�ċÌł���̂Ō��ʓI�ɋ����g�D�ɋ߂��g�D��悷�邱�Ƃ�����B
�@�@Cu-Pb�AAl-Pb�AAl-In�Ȃǂ�����B
�@�@

�@�E�peritectic�g�D
�@�@�@��͉t���ƌő�����ʂ̌ő����������锽����
�@�@�@�@L�{�������@
�@�@�ő������ő��������͂g�D���`������B
�@�@Ni-Al�AFe-C�ȂǂŌ�����B�@
�@�@

�@���Ìł̔��̗n�Z�ߒ��ɂ����Ă͈�v�n�Z�i���v�n�Z�A���a�n�Z�ACongruent Melting�j�ƕ���n�Z
�i�s��v�n�Z�A�a�n�Z�AIncongruent Melting�j����������B
�@�@���������Z�_�Ōő̂Ɠ����g���̉t�̂ɂȂ�ꍇ����v�n�Z�ł���A�����I�ɗn�Z�܂蕪�����ėn�Z���ő̂ƈقȂ�
�@�ʂ̌ő̂Ɖt�̂ɂȂ�ꍇ������n�Z�ŒP�����琬�ɂ����Ė��ƂȂ�B
�@�@����n�Z�������͈�ʂɕ�����ł���B
�@�����ʏ��o�i�������jfractional crystalization��p
�@�@��ɍz���w�ŁA���o�����������c�t���番������i�����n�O�ɏo��j���Ƃɂ�蕽�t�ƈقȂ錋�����������Ă������ۂ������B
�@�@
�i�S�|�Q�j�@�����g�D�̕���
�@�����g�D�̕��ނɂ͂������̕��@������A���Ƃ���
�@�@�`�Ԃ���
�@�@�@����normal�����i���邢�͋K��regular�����j�ƈُ�anomalous�����i���邢�͕s�K��irregular�����j�Ƒމ�degenerate�����B
�@�@�M�͊w�I��
�@�@�@�m���t�@�Z�b�g�E�m���t�@�Z�b�g�����A�m���t�@�Z�b�g�E�t�@�Z�b�g�����A�t�@�Z�b�g�E�t�@�Z�b�g�����B
�@�@�����@�\����
�@�@�@���������A���������B
�Ȃǂƕ��ނ����B

�i�S�|�Q�|�P�j�@Brady�̕��ށi�P�X�Q�Q�N�j
�@�\�ʒ��͂���ɕ��ށB
�@�N���X�P�D�@����globular
�@�@�@�������͍������قȂ�\�ʒ��́BCd-Sn�ACd-Pb�ACu-Ag�AZn-Bi���B
�@�N���X�Q�D�@�w��lamellar
�@�@�@�������͍����Ăقړ������\�ʒ��́B�قړ����������BPb-Sn���B
�@�N���X�R�D�@�p������angular
�@�@�@�`�D�@������Ⴂ�\�ʒ��́BSb-Pb�APb-Bi�ASn-Bi�ACd-Bi���B
�@�@�@�a�D�@����������\�ʒ��́BAg-Pb�AAg-Bi�AAl-Sn�ACu-Bi�ACu-Pb���B
�@�N���X�S�D�@������crystalline
�@�@�@�������̕\�ʒ��͂͒Ⴂ�BSb-CuSb�B����������ɗǂ�������B
�i�S�|�Q�|�Q�j�@Portevin�̕��ށi�P�X�Q�R�N�j
�@�`�Ԃ��番�ށB
�@�^�C�v�T�@�K������
�@�@�@�ЂƂ̐����̃}�g���b�N�X�ɑ��̐������U�݁B
�@�@�@Sn-Cu�ASn-Co���B
�@�^�C�v�U�@�f���h���C�g�܂��͊[��skeleton�i���A�ł��������������̐������x��E��ł���j
�@�@�@Ag-Sb�AMg-Cu�AMg-Si�ABi-Pb���B
�@�^�C�v�V�@�����Q��colony�܂��͕��G��complex grains
�@�@�@spherical�i����j�Afan-like�i���j�Aparallel-clustered�i���s���W�j varieties�ɕ����ށB
�@�@��Portevin�̕��G��complex grains�͓����ɋ������q���������̑��ʑ̂ł܂������Q��colony�Ƃ��Ă�邪�A�זE��cellular������
�@�@����邱�Ƃ�����B
�@�^�C�v�W�@granular
�@�@�@�����ɂ͌����Ȃ��B
�i�S�|�Q�|�R�j�@Chadwick�̕���
�@�@�A�������A�s�A�������A�点���ɕ��ށB
�@�@Gupta��Phase Equilibria in Materials�ɂ��ڂ������ނł�
�@�E�A������
�@�@�@�@���������������ɘA�����Ă���B
�@�@�@�������i�w��j����
�@�@�@���b�h��i�_��j����
�@�@�@�Z���i�זE�j���i�R���j�[��j
�@�@�@�@�@�����Q��colony���邢�͍זE��cellular�����̓Z���ɑ����i�P�O�|�P�O�O�j�̃����������傫�ȗ��ł���B
�@�@�@�点��
�@�@�@�@�@�Q�����͂ߍ��܂ꂽ���Z���Ƃ��đ��݁AZn-Mg�ȂǁB
�@�@

�@�E�s�A������
�@�@�@�@���̘A�������Ȃ��A�}�g���b�N�X�Ƀo���o���ȗ��q�����U�����`�ő��݁B
�@�@�@�j��acicular
�@�@�@�m�W���[����i���j
�@�@�@������chinese script
�i�S�|�Q�|�S�j�@Scheil�̕��ށi�P�X�T�S�N�j
�@�@�n�����̑̐ϔ�u�e�ɂ�镪�ށB
�@�E����nomal�����i�K�������j
�@�@�̐ϔ䂪�߂��B�m���t�@�Z�b�g�E�m���t�@�Z�b�g�����B
�@�@��������@
�@�@���b�h��
�@�E�ُ�anomalous�����i�s�K�������j
�@�@�̐ϔ䂪�傫���قȂ邩�A�������������Ȉٕ����������B
�@�@�m���t�@�Z�b�g�E�t�@�Z�b�g�����B
�@�@�s�K���Ȃ����j�[�h����B
�@�E�މ�degenerate����
�@�@���틤�����邢�ُ͈틤���̂悤�ȋ��������ɂ��g�D�������Ȃ��A�}�g���b�N�X���ɑ�Q�����قڋψ�ɕ��z������Ԃ�����
�@�����n�g�D���w���B�{�������@�\���������������Ƌ�ʂ����Ȃ��Ȃ��Ă���B
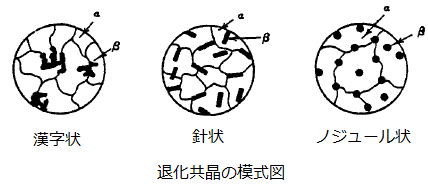
�@�@��Ȍ`��́A�m�W���[����i���j�A�j��acicular�A������chinese script
�@
 �iIntroduction to Solid State Chemistry����j
�iIntroduction to Solid State Chemistry����j�i�S�|�Q�|�S�j�@Jackson�̗n�Z�G���g���s�[���r�ɂ�镪�ށi�P�X�U�U�N�j
�@Jackson�͗n�Z�G���g���s�[���r�ɂ���ĂR���ށA�����Taylor���g��B
�@Taylor�͗n��solution�G���g���s�[���g�p���A�Q�R�i�^mol-K����Ƃ����B
�@�E�m���t�@�Z�b�g�E�m���t�@�Z�b�g�����i���틤���j
�@�@�@��������G���g���s�[�A�Q�R�@�i�^mol-K�ȉ�
�@�E�t�@�Z�b�g�E�m���t�@�Z�b�g�����i�ُ틤���j�@�@
�@�@�@���G���g���s�[�ƒ�G���g���s�[
�@�E�t�@�Z�b�g�E�t�@�Z�b�g����
�@�@�@�s�K�������B
�@�@�@���������G���g���s�[�A�Q�R�@�i�^mol-K�ȏ�
�i�S�|�Q�|�T�j�@Kurz ��Fisher�̕��ށi�P�X�W�X�N�j
�@�@Jackson�̍r���p�����[�^�[���Ɨn�����̑̐ϔ�u�e�ɂ�镪�ށB
�@�@�@�@�@�@�@�@�m���t�@�Z�b�g�E�m���t�@�Z�b�g�����@�t�@�Z�b�g�E�m���t�@�Z�b�g�����@
�@
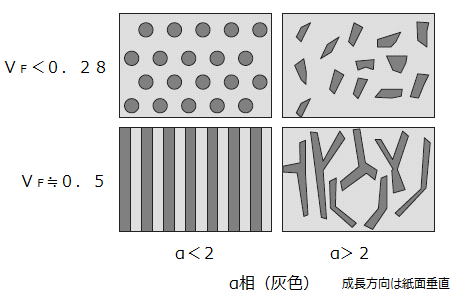
�i�S�|�Q�|�U�j�@Croker��̕��ށi�P�X�V�R�N�j
�@�n���G���g���s�[���r�Ɨn�����̑̐ςu�e�ɂ�镪��
�@�K��������lamellar�A�K�����b�hrod�A�}��broken�������i�Ƒ@��fibrous�j�A�s�K���A���Gcomplex�K���A��quasi�K���ɕ��ށB
�@�@���Gcomplex�K���F������regular��cellular��cellular�Ԃ�irregular�B
�@�@��quasi�K���Fplate��rod�̑g�ݍ��킹�B
�@�@�@�@�@�i�������x�P�O�S����/���j

�@�u�e���P�O���Ŏ}�܃���������s�K���Џ�flake�\���ɕω����A��Q�O���ŕ��G�K���\���ɕω��A�X�ɂu�e���傫���Ȃ�Ə�i�K���\���ƂȂ�B
�@�@�@�@�@�@
�@�����Əڂ������ނł͋K��������lamellar�A�K�����b�hrod�A�}��broken�������A�s�K���A���Gcomplex�K���A��quasi�K����
�点��spiral�A����globular�Ƃ������ނ��Ȃ����B
�i�S�|�Q�|�V�j�@Spengler�̕��ށB
�@�@�Q���̑̐ϔ�̂ق��ɗZ�_�̊W���������B
�@�@�Ɓ��i�s�P�|�s�d�j�^�i�s�Q�|�s�d�j�@�@�@�s�P����n�Z�����̗Z�_�A�s�Q�����n�Z�����̗Z�_�A�s�d�������_
�@�@�@���틤���F�O�D�P���Ɓ��P
�@�@�@�ُ틤���F�O�D�O�P���Ɓ��O�D�P
�@�@�@�މ������F�Ɓ��O�D�O�P
�i�S�|�Q�|�U�j�@Sundquist�AMondolfo��̗��_
�@�s�����̑������`�����̂ǂ��炩�̊j�����𑣐i���ُ틤���g�D�̌`���K��v���ƂȂ�B
�@���틤���͋��������A�����e�X�̊j�����𑣐i���������i���������j�A�ُ틤���ł͕s������
���҂̊j�����𑣐i���A�ɒ[�ȏꍇ�A�������������̃n���[�Ɉ͂܂�A�މ��g�D�ƂȂ�B
�i�S�|�R�j�@�����Ìł̗��_
�@�@Zener�̓��������������Ń������Ԋu�Ɂv�Ɛ������x�u��
�@�@�@���Q�u�����
�@�Ƃ����B
�@�@Hunt��Jackson�͂���ɂ��Ĉ�ʗ��_�𗧂Ă��B
�@�EHunt��Jackson���_�Ƌ���cooperative�icoupled�j����
�@�@
�@�@���ʌʼnt�E�ʁi�R�d�_�j���`�����A���������Ɛ��������ɗn�����������Ȃ��琬���B
�@�@�����̕��ω��x�͓������������i�����j�������郢�s�����s�������s��
�@�@���s�����s���{���s���Ƃ��Čv�Z�B
�@�@���s���j�P�ɂu�{�j�Q�^��
�@�@���Q�u���j�Q�^�j�P�i�����j
�@�@���s�Ɂ��Q�j�Q�i�����j
�@�@���s�Q�^�u���S�j�P�j�Q�i�����j
�@�@

�@�ETrivedi�AMagnin�AKurz���_
�@�@�y�N�����oe�͋��������̊E�ʐ��������̈�ʓI�]���ʂŁAHunt��Jackson���_�ł͂P�����ɏ��������Ȃ킿�A�����Ԋu�i�Ɂj�͊g�U����
�@�����ɏ������A�E�ʉߗ�p�͊E�ʑg�����قڋ����g���ɓ��������炢�ɏ������Ɖ��肳��Ă���B
�@�@Hunt��Jackson���_�͐������x���������ꍇ�ɓK�����A�傫���ꍇ�͊g�U�����͏������Ȃ�A�ߗ�p�͔��ɑ傫���Ȃ�A�y�N�����oe�͂P�ɋ߂Â��A
�@Hunt��Jackson���_�͔j�]���A���Q�u���͒萔�łȂ��Ȃ�B
�@�E���������烍�b�h�ւ̕ω��iChadwick�̐����j
�@�@�s�����̌��ʂŐ����A�Y���s�����̃����ƃ����̕��z�W�������Ȃ�قȂ�Ƒg���I�ߗ�p������̑��ő傫���A
�@���̑��̃������͕���B
�@�@����AHunt�͒[�ʂł̕�����ȗ��E�ʂƌ��т����Z�����E�ł̐��������̕ω��̂����ɂ����B
�@

�@�@���������烍�b�h�ւ̕ω��̋@�\�iChadwick�̐����j
�@�E�����E�ʂ̕s���萫
�@�@�Q�����n�̋��������͕��ʓI�E�ʂŐ������邪���������ɂȂ�ƕ��ʓI�Q���E�ʂ͕s����ƂȂ�A���ʂ���Z����cellular�i�R���j�[�j�A
�@�X�Ƀf���h���C�g��ƂȂ�B
�@

�@�EFisher-Kurz�̕���branching��������
�@�@�t�@�Z�b�g���ٕ̈����������͊w�B
�@�@�s�K�������ł͎�X�̃������̐��������͕��s�ł͂Ȃ��i�t�@�Z�b�g���ٕ̈����j�A�������郉�����ł͋Ǖ��Ԋu�͌������A
�@���U���郉�����ł͍L����B
�@�@�Ɍ��ł͎������郉�����͈����������A���U���郉�����͂Q�ɕ���B����̋N����ő啝�����߂������B
�@�@

�@�E�U��oscillatory���[�h
�@�@�m���t�@�Z�b�g���̃��������͍ő�l�ƍŏ��l��U������B
�@�@

�i�S�|�S�j�@��������competitive gowth�ƃJ�v���h�E�]�[���i�����̈�j
�@�E��������competitive gowth
�@�@�@�f���h���C�g�Ƌ����̋����ƃJ�v���h�E�]�[���i�����̈�j
�@�E�J�v���h�E�]�[��coupled zone�i�����̈�j
�@�@�@�����͋����g������O�ꂽ�g���ł������g�D���`�����₷���A�������������₷���̈���J�v���h�E�]�[���Ƃ����B
�@�@�Ώ̌^�@�@�Z�_���߂��A�����g�������Ă��Ȃ��ꍇ�B
�@�@��Ώ́i�ΌX�jskew�^�@�@�Z�_�����傫���A�����g������Z�_�������ɕ��Ă���ꍇ�B
�@

�i�S�|�T�j�@���������Ƌ�������
�@�����̋Ìłɂ͋��������̂ق��ɕ�������������B
�@���������i���������j�͑މ������ȂǂƂƂ��ɋ��������Ɍ�����悤�ȋ����g�D�������Ȃ��B
�@�{���A�މ������͌`�Ԃ���̖����ŕ��������͐����@�\����̖����ł��邪�`�ԓI�ɂ͗ގ����邽�ߋ�ʂ���Ȃ��Ȃ��Ă���B
������divorced������
�@�@���������i�������A���b�h��j�Ɍ�����悤�Ȓ����z�u���Ȃ��A�����ƃ������X�ɔz�u������X�̋����\���������A
�@�����_���͂��ꂽoff eutectic�g���̋����i����̑��̑̐ϔ䂪�������j�Ń������j�����̂��ߑ傫�ȉߗ�p��K�v�Ƃ��邽�߁A
�@�������t�����̉�����������I�Ƀ������`�������܂Ő�������邱�Ƃɂ�萶����Ƃ����B
�@�@���������ł͋ÌőO���Ń����ƃ����̋��ʂ̌ʼnt�E�ʌ`���Ɨn���̌��������݂����A�������݂��ɓƗ����Đ�������B
�@�@���������̋����ł̓����ƃ����͓����ɐ������邪���������ł͕ʁX�ɐ�������B
�@�@���������ł͏����̃f���h���C�g�Ԃ̑傫�ȋ�ԁi�|�P�b�g�j�ɋ����g�D���������邪�A���������ł͏����̃f���h���C�g�Ԃ�
�@�����ȋ�Ԃɕ����������N��B
�@�@���̋@�\�ɂ��`�������\���͎�X�̌`�Ԃ��Ƃ蓾�A��{�I�Ƀ����̃}�g���b�N�X�Ƀ���������ɕ��U�����A�m�W���[���i��j��A�j��A
�@������chinese script�ȂǂƂȂ邪�A�����`�Ԃ̌`���͏����̃f���h���C�g�ɂ���Č`�������f���h���C�g�Ԃ̏����ȋ�Ԍ`��ɋK�肳���B
�@
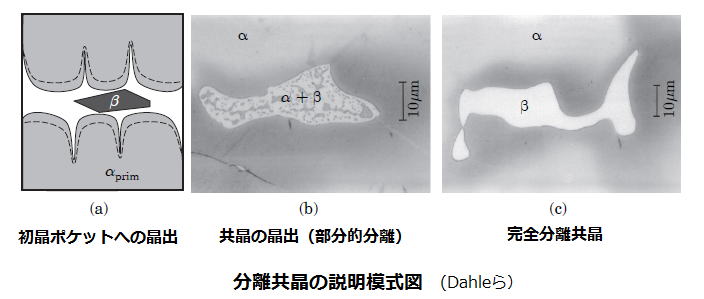
�@�@�܂��ʂ̐��ł͏������̃f���h���C�g���ʐϓI�ɑ����A���������̃f���h���C�g�̏����ȋ�Ԃ̌`�������ꍇ�A�����̃�������������
�@�D��I�Ɍ`������邽�߁A���������c���ꂽ��ԂƂȂ�Ƃ������B
�@
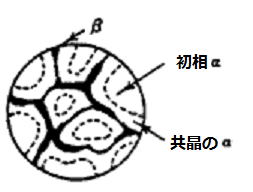
�@�@���{���A�މ������͌`�Ԃ���́A���������͐����@�\����̖����ł��邪���ʓI�Ɏ����g�D�������A�܂������@�\�����m�łȂ����߁A
�@�މ������A���������̋�ʂ͖��m�ł͂Ȃ��B
�@�E�����U���Ioscillatory����
�@�@������Ìłł̕��������Ń����ƃ����̌��݂̊j�������J��Ԃ���邱�Ƃ�U���I�Ƃ����я�\���ƂȂ�B
�@�@�i�ÌŌo�H�͔t�O�Ձj
�@�E����symbiotic�����i�������������j
�@�@���������͂P�ϐ������n�i�R�����n�j�̓���Ȑ����^�C�v�ŁA�����E�ʂƐ����ɂ�����t���M���b�v��ʂ��Ă̊g�U�ɂ��n���������s���Ȃ���A
�@���ʂ̌ʼnt�E�ʂ͌`�������i�����ƃ����͉t���ɂ��u�Ă���j�ɓ����ɐ�������B
�@�@�i�ÌŌo�H�͂قڕ��t�O�Ղ����ǂ�B�j
�@�@���̂悤�Ȑ����͏������ւ̐ڎ�܂̓Y���ɂ���ĉ\�ƂȂ�B
�@�@������Ìłł͕���ȃ}�g���b�N�X���̑O�ʂɏ��������j���������q�ɐ������A���q�ƈړ�����E�ʂɓ����͂ɂ�藱�q�̔r���ƕ������݂̔z�u
�@�����܂�A���̘A���̌J��Ԃ��őя�\�����`�������B
�@

�@�@�@�@�@�@�@�ihttp://adsabs.harvard.edu/full/2001ESASP.454..565H����j
�@�E�n���[halo�ƕ�������
�@�@�@�������Q���̑w���͂�ŋ������番�����Ă���Ƃ���Q���̑w���n���[halo�i���邢�̓G�����F���[�venvelope�j�Ƃ����B
�@�@�@
�@�@Sundquist��ɂ��n���[halo�`���̐����B
�@�@�@�����̔ݓI�j����������b�A�������������قƂ�ljߗ�p�Ȃ��Ɋj����������Ƃ���A�����̓������j���������ɂ����B
�@�@�@�ߋ����������t�������x�ɂȂ�Ə����������o���A�t�����ɉ����đg�����ω�����B�������������j���������ɂ����ƁA�t���g����
�@�@�t�����̉����̉����ĕω������鉷�x�ʼnߗ�p���傫���Ȃ胿�������o���A�����̓����̎��͂Ƀ����̃n���[���`������B
�@�@�@�����̐����ŋ����g���܂Ŗ߂�A�������������n�߂�B
�@�@�@�����������ł͉t�������x�ɂȂ�Ə����������o���A���������o����܂ŁA�t���g���͉t�����Ƃ��̏����艄���ɉ����ĕω����A
�@�@���鉷�x�ʼn߃��������o����A�����������������j�������₷���ƁA���̉��x�͋������x�ɋ߂��A�����̓n���[�Ƃ��Đ������A�����g���ɂȂ�ƁA
�@�@�������������n�߂�B
�i�S�|�U�j�@���S�Ƌ���
�@��v�Ȓ��������ł���`���|�r���n�Ƃe���|�b�n�̓m���t�@�Z�b�g�|�t�@�Z�b�g�����ɑ����A��X�̓��قȌ`�Ԃ������B
�@�e���|�b�n�ɂ͂Q�̋����n�̂e���|�O���t�@�C�g�i�����j�Ƃe���|�J�[�o�C�h�i�e���R�b�j������B
�@�J�[�o�C�h�`�����f�i�b���A�l���A�v���j�͔����S���𑣐i���A�J�[�o�C�h���`�����Ȃ����f�i�r���A�b�A�`�����j�͂˂��ݒ��S���𑣐i����B
�@�܂��������A�������A�Y�����A�_�����A�����ԉ��������͍������o�j�ƂȂ�˂��ݒ��S���𑣐i����B
�@

�@�@�@�@�e���|�b�n��Ԑ}�i�����F�e���|�Z�����^�C�g�n�A�_���F�e���|�����n�j
����Ȓ��S��
�@�E�����S white cast iron
�@�@�@������e���|�J�[�o�C�h�n�Ìł̌��ʐ����A�I�[�X�e�i�C�g�ƃJ�[�o�C�h�i�Z�����^�C�g�j�̔��F�����i���[�f�u���C�g�j������B
�@�@�@�ŏI�I�ɃI�[�X�e�i�C�g�̓p�[���C�g�A�t�F���C�g���ƂȂ�B
�@�@�@�������iedgewise�����j�Ɩ_��isidewise�����j�̂Q�^�C�v�̋����\����������B
�@�@

�@�@���[�f�u���C�g�����̖͎��}
�@�E�˂��ݒ��S gray cast iron
�@�@�@����e���|�O���t�@�C�g�n�Ìł̌��ʐ����A�I�[�X�e�i�C�g�ƃO���t�@�C�g�̊D�F����������B
�@�@�@��p���x�ŃO���t�@�C�g�̌`��ω��B
�@�@�@�ŏI�I�ɃI�[�X�e�i�C�g�̓p�[���C�g�A�t�F���C�g���ƂȂ�B
�@

�@�@�@�@�@�@�@�@�@�e�f�F�Џ��A�b�f�F�b�u�����A�r�f�F������
�@�@�@�g���A���x���z�A�������x�̉e���̂e���|�b�|�r�������̌`�Ԗ͎��}
�@�E�܂��璒�S mottle cast iron
�@�@�@�����S�Ƃ˂��ݒ��S�̒��ԑ̂ŃO���t�@�C�ƃJ�[�o�C�h��L����B
�@���_�N�^�C��ductile���S
�@�@�@�������������������́B
�@���b���S�i�}���A�u��malleable�j
�@�@�@�����S�i�p�[���C�g�E�}�g���b�N�X���ɃJ�[�o�C�h�j��M�������J�[�o�C�h�������A�Ă��߂�temper�����Ƃ������́B
����X�Ȃe���|�O���t�@�C�g�n���S��
�@�E�Џ�flake�������S
�@�@�����̌`��ł`�^����d�^�ɕ��ނ����B
�@�@�`��E���@�͑g���A�ߗ�p�x�A�ڎ�܁i���ʓY�����j�ɂ��B
�@�@�`�^�F�ψꕪ�z�A�������z��
�@�@�a�^�F���[�[�b�g�i�~�ԏ���j��W���A�������z��
�@�@�b�^�ݏd�Џ�A�������z��
�@�@�c�^�F�f���h���C�g�ԕΐ́A�������z��
�@�@�d�^�F�f���h���C�g�ԕΐ́A�D��z��
�@

�@�E�b�ucompacted vermicular�������S �@vermicular�F����
�@�@�@����ƕЏ�̒��Ԍ`��B
�@�@

�@�E����spheroidal�������S�i�_�N�^�C��ductile���S�A�m�W�����[nodular���S�j
�@�@�@�l���A�b���A��y�ނȂǂ̓Y���ɂ��B
�@�@�@���������S�͕��������@�\�ɂ��ƍl�����Ă���B
�@�@�@�����A�����ƃI�[�X�e�i�C�g�͕ʁX�Ɂi�ꏊ�Ǝ��ԁj���o���i���������j�A���鋅���ł͎��͂ɃI�[�X�e�i�C�g�k���`������A
�@�@���̋����̓I�[�X�e�i�C�g�k��ʂ��Ă̊g�U�ɂ�萬�����n���[���`�������B
�@�@

�@�@�@�������̐����̖͎��}�i���������ƃn���[�j
�i�T�j�@�Ìʼnߒ��̐���
�i�T�|�P�j�@�_�C�L���X�g�Ɨn���b���@
�@�E�_�C�L���X�g
�@�@�@�傫�Ȉ��́i��MPa�`���P�O�OMPa�j�ŗn�������^���֎ˏo�B
���_�C�L���X�g����
�@�@�_�C�L���X�g�ɗ��p������ȍ����͂`���A�y���A�l�������ł���B
�@�@�Z�_�@�y���F�S�P�X�D�T���A�l���F�U�T�P���A�`���F�U�U�O��
�@�E�n���b���i���������j
�@�@�@�n���������i���P�OMPa�j�ʼn��������܂܋Ìł�����B
�@�@�i�_�C�L���X�g�ł͈��͂͋��^���֎ˏo���邽�߂ɏ�����j
�i�T�|�Q�j�@���Ìʼn��H�Ɣ��n�Z���H
�@�E���Ìʼn��H�i���I�L���X�g�j
�@�@�������ʼnt������Ԃŋ@�B�I���邢�͓d���I���@���ɂ��h�a���s������������}�g�D��j�ӂ��A
�@����̌ő������Ɖt�������Ƃ��ψ�E���ׂ������I�ɕ��U�����ʼnt������ԂƂ���������B
�@�@�ÌŎ��k���������A�ώ��ȗ���g�D��������A�}�N���ΐ͂����Ȃ��A���^�̔M���ׂ��������Ȃǂ�
�@���_������B
�@�E���n�Z���H�i�`�L�\�L���X�g�j
�@�@���Ìʼn��H�̂悤�ɂ��Čő��������Ɖt�������Ƃ��ψ�E���ׂ������I�ɕ��U�����ʼnt������Ԃɂ��A
�@������������S�ɋÌł������̂��ĉ��M���Čʼnt������ԂŒ�������B
�i�T�|�R�j�@�������
�@�Ìő��x�i�ړ����x�j�Ɖ��x���z�i�F�̉��x���z�j�𐧌䂵�Ìł�������ɐ��䂷�������Ìł�Ni�����
�ōs����B
�@�܂������g�D�̈�����ÌłȂǂ���������Ă���B
�i�T�|�S�j�@�}��ÌŁ@
�@�����̉�]���[���ɋ����t�̂˂���Ȃǂ̕��@�ɂ��t�̋}��@�ŋ����̃A�����t�@�X���������ł���B
�@
�i�T�|�T�j�@���e��ÌŁ|���V�@
�@���e��Ìł�����������̂Ƃ��ĕ��V�@������B
�@�d���A�K�X�W�F�b�g�A�����g�A�Ód�A����@�Ȃǂ𗘗p���Z�t��ێ�����B
�@���e��n�Z�ł͑傫�ȉߗ�p��������B
�i�T�|�U�j�@�����̋ÌŖc��
�@
�@�a���A�r���͋Ìłɍۂ��c������B
�@�a���͂T�O�|�U�O���ŋÌŎ��k�O�ƂȂ�a���|�S�Q�r���Ȃǂ����p�����B
�i�U�j�@�͏o�@
�@�����ł͐͏o�Ƃ͌ő��ł̐V�������̐����Ɖ�����B
�@�i�t������̌ő��̐����͏��o�A���邢�͏��́A�������t���i�n�t�j����̌ő��̐�����͏o�Ƃ����ꍇ������B�j
�@�ő��ϑԗ���Johnson-Mehl-Avrami�̎�
�@�@�u���P�|exp�i�|�������j
�@�ŕ\�킳��A���F�A�u���~�w���͐����@�\�ɑ���������B
�i�U�|�P�j�@�X�s�m�[�_���Ȑ��ƃo�C�m�[�_���Ȑ�
�@�ߖO�a�ŗn�̂���V������������ɂ͊j�����|�����^���������X�s�m�[�_������������B
�@�Q���������������^�̏�Ԑ}�����Ƃ��ŗn�̂̎��R�G�l���M�[�̑g���ˑ����͏�ɓʂ�W�`�Ȑ�
�i�Q�̋ɏ��ƂP�̋ɑ�����j�ƂȂ苤�ʐڐ��̓�̐ړ_�̊ԁi�n��x�M���b�vmiscibility gap�j��
���������N����B
�@���̐ړ_�̋O�Ղ��o�C�m�[�_��binodal�i�n��x�M���b�v�j�Ȑ��ł���A���R�G�l���M�[�̕ϋȓ_�̋O�Ղ�
�X�s�m�[�_��spinodal�Ȑ��ł���B�@
�@���R�G�l���M�[�̂P�K�����͑��̕��t��Ԃ́A�Q�K�����͈��萫�̖ڈ��ƂȂ�B
�����nexsolution
�@�z���w�A��Ίw�Ȃǂł͉ߖO�a�ŗn�̂̕����A�V���͏o�𗣗n�Ə̂��A���͂��܂߂Ă���B
�@���͂ɂ�郉�����\����A��intergowth�Ƃ��̂���B
�@�ߖO�a�ŗn�̂���̐V���͏o�͕ꑊ�ɑ��Ĉ��̌����w�I�W�������ċK���I�ɐ͏o����̂ŕ�ł�
�A�X�e���Y���A�V���g�����V�[�A�V���[�Ƃ��������ۂ���B
�@�@�A�X�e���Y���i�X�^�[���ʁA���ʌ��ʁj�E�E�E�X�^�[�E���r�[�A�X�^�[�E�T�t�@�C�A�ȂǂɌ����錻�ہB�s�����i�s���n�Q�j�͏o�ɂ��B
�@�@�V���g�����V�[�i�L���b�c�A�C���ʁA�ύʌ��ʁj�E�E�E�L���b�c�E�A�C�i�N���\�x�����j�A�ȂǂɌ����錻�ہB�s�����͏o�ɂ��B
�@�@�V���[�i���ʁA�A�f�������b�Z���X�j�E�E�E�������\���ɂ��A���̐����i�I���\�N���[�X�j�Ƒ����i�A���o�C�g�j�ւ�
�@���́i�p�[�T�C�g�������j���L���B
�@�@�@
�@�@覐Ɍ�����E�B���h�}���V���e�b�e���g�D���m���e�������̂m���i�e�[�i�C�g�j�Ƃe���i�J�}�T�C�g�j�̋��͂ɂ�郉�����g�D�B
�i�U�|�Q�j�@�X�s�m�[�_������
�@�X�s�m�[�_���Ȑ��̓����ł͔M��炬�ɂ�萶�����Z�x�ω��͌n�̎��R�G�l���M�[��ቺ�����ŗn��
������ŁA�����ȔZ�x�ω����瑊�������n�܂�A���I�Ɏ����I�ɂ�炬���傫���Ȃ葊��������������B
�@�X�s�m�[�_�������ł͔Z�x�ϓ��̔g���ɑΉ����������\���i�ϒ��\���j�����B
�@Cu-Ni-Fe�AAl-Zn�AAu-Ni�ȂǂŌ�����B
�@�X�s�m�[�_������������g�U�iuphill diffusion�A�t�g�U�j�̂P��ł���B
�i�U�|�R�j�@�j�����|�����^�������@�@
�@�o�C�m�[�_���Ȑ��ƃX�s�m�[�_���Ȑ��̊Ԃł͊j�����|�����^���������N����B
�@���͈̔͂ł͔M��炬�ɂ�萶���������ȔZ�x�ω��͌n�̎��R�G�l���M�[���㏸������̂ŕs����ł���
�Z�x�ω��͏��ł����̌ŗn�̂ɂ��ǂ邪���炩�̂��������ň���g���ɋ߂��͏o�j���o���i�������ԁj
����Ύ��R�G�l���M�[�͒ቺ�����������i�s����B
�@�E�I�X�g�����h����
�@�@�ꑊ�ɑ傫�ȗ��q�Ə����ȗ��q�����U���Ă���Ƃ������ȗ��q�����k�E���ł��傫�ȗ��q���������錻�ۂ��I�X�g�����h�����Ƃ����A
�@����͕ꑊ�ւ̗n���̗n��x�����a�Ɉˑ����邱�Ƃɂ��B
�@�@���Ȃ킿Thompson Freundlich�̎�
�@�@�@�@�b�����b��exp�i�Q�l���^���q�s�ρj�@�@
�@�@�@�@�b���F���a���̗��q�̗n��x�A�b���F������̗��q�̗n��x�A�l�F�n���̕��q�ʁA���F�\�ʒ��́A�ρF���x
�@��藱�a�̏��������̂قǗn��x���傫���B
�@�@�܂����q������Lifshitz-Slyozov-Wagner�̗��_�ł�
�@�@�@�����R�|���O�R���j���^�s�@�@�@�����A�O�F���Ԃ��A�O�ł̕��ϗ��q�a�@K���W��DV���Q�����^�X�q�@�ЁF�E�ʃG�l���M�[�AD�F�g�U�W���AVm�F�����̐�
�@�ߖO�a�ŗn�̂���̐͏o�ɂ��A���͏o���s�A���͏o�i���E�����^�͏o�j������B
�@�E�A���͏o
�@�@�A���͏o�͗����ɕ��U���Đ͏o���A�ꑊ�̕��ϑg���͏��X�ɕ��t�g���ɋ߂Â��Ă����B
�@�E�s�A���͏o�i���E�����^�͏o�j
�@�@�s�A���͏o�͗��E����ߖO�a�ŗn�́i�����j�Ɍ������ė��E�ړ����Đ͏o�����ƕ��t�g���̑������������g�D�i�w��j

��悵�Ȃ��琬�����A�ߖO�a�ȑ����f�͗��E�ړ��ɂ���ĊE�ʂ���|�����܂őg���͕ω����Ȃ��B
�@�i�ړ����闱�E�ɂ͕��t�g���̃��ƉߖO�a�ȃ��f�őg���̕s�A��������B�j
�@�������g�D�����m�W���[���Ə̂���B
�@�i�������g�D��悷��ʂ̗�͋��͂ł���B�j
�@�E���͏o�i���j�тo�e�y
�@�@���E�t�߂ɐ͏o���̑��݂��Ȃ��̈恁���͏o�i���j���������邱�Ƃ�����B
�@�@����͗��E���n�����E�i�s�ώ��j�����̏�j�̑|�����߁i�V���N�j�Ƃ��ē������ߎ��ӂł���炪�͊����邽�߂Ƃ����B
�i�U�|�S�j�@����
�@�ő�����̐͏o�ŋÌłł̋����ɑΉ�����̂����͂ł���B
�@���͕ϑԂł͊g�U������Z������悤�ɂQ��ނ̐����������݂ɋK���I�ɔz���g�D���`�������B
��\�I�Ȃ̂�Fe-Fe3C�n�̃p�[���C�g�ϑԂł���B
�@��Fe�i�������j����Fe�i�������j�{Fe3C
�@���i�t�F���C�g�j����Fe3C�i�Z�����^�C�g�j���͔�̊e�������݂ɔz���������\�����Ƃ�B
�i�U�|�T�j�@�ΐ́i���m�e�N�g�C�homonotectoid�j�A��́iperitectoid�j
�@���ꂼ��Ώ��A��ɑΉ������ΐ́i���m�e�N�g�C�h�j�A��͂�����B
�@�ΐ́imonotectoid�j�@�@Al-Zn�ANb-Zr�Ȃ�
�@�@���P�����Q�{��
�@��́iperitectoid�j�@�@Cu-Si�Ȃ�
�@�@���{������
�i�U�|�U�j�@�͏o�ߒ��̐���@�@
�@�E�͏o�d���i�����d���j
�@�@�n�����q�̌ŗn���̉��x�ω��i�ߖO�a�ŗn�́j�𗘗p���Ĕ��ׂȐ͏o�����`�����邱�Ƃɂ�镪�U����
�@�𗘗p�����͏o�d���^����������Al�������L���ł���B
�@�@�͏o���Ƃ��Ă͋����ԉ����������p����邱�Ƃ������B
���f�o�]�[��
�@�@�`���|�b�������̎����d���ł͎����ߒ��ŕ��t��Ԑ}�ɂȂ��f�o�]�[���ƌĂ��͏o���������邱�Ƃ��m���Ă���B
�@�@����̓A���~�j�E�������́i�P�O�O�j�ʂɂb�����q���������Ĕ�ɏW���������̂Œ��a���P�O�����łP�`�Q���q�w���Ȃ��Ƃ����B
�@�@�`���|�b�������̂ق��`���|�l���A�`���|�y���A�`���|�`���A�l���|�y�������Ȃǂɂ�������B
���}�g���b�N�Xmatrix�ƕꑊparent phase
�@�@�����i�ޗ��E�����j���͏o�����邢�ّ͈��ȂǕ����̑����܂ޏꍇ�A��v�ȑ����}�g���b�N�X�Ƃ����B
�@�@�}�g���b�N�Xmatrix�̌��`�̓��e����Łu�q�{�A��́v�̈ӁB
�@�@��ʓI�ɂ͊�A�����ł͊�n�A��́A�ꑊ�ȂǂƂ����ꍇ������B
�@�@�͏o���̕�̂̏ꍇ�͕ꑊparent phase�Ƃ����ꍇ�������B
�@�@�`���̊ϓ_�łȂ���Ԃ̏ꍇ�̓}�g���b�N�X�ɑ��_�݂��鑊�U���ƌ����B
�������Ɣ�
�@����coherent
�@�@�ꑊ���Ő����Ђ��݂������E�ʂ͂Ȃ��B
�@�@�����͏o
�@�@�@�ꑊ�ƌ����i�q�̘A������ۂB
�@�@�@�͏o���̑傫���A�����i�q�̑傫�����W����B
�@�@
 �@�@
�@�@�@�@�@�@�@�@�@�@�@�@�@�@���͏o�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�����͏o
�@��noncoherent
�@�@�ꑊ�i�}�g���b�N�X�j�Ɛ͏o�����E�ʂ����B
�@������
�@�@�E�ʂœ]�ʂ����݁B
�@�E�i�m�����E�i�m�R���|�W�b�g
�@�@�͏o�ߒ��̐���Z�p�Ƃ��Ă͏]������͏o�d���i�����d���j�����邪�V���������Ƃ��Č����g�D��
�@�i�m�X�P�[���̃T�C�Y�����i�m�����A�i�m�R���|�W�b�g�̍쐻����������Ă���B
�@�@��\�I�ȕ��@�̓A�����t�@�X�̔M�����ł���B����ޗ��⎥�Ŏ��p���Ⴊ����B
�i�V�j�@�ő��ϑ�
�i�V�|�P�j�@�K���E�s�K���ϑ�
�@
�@�ߖO�a������̑������͊g�U�ϑԂł��邪�A�����g�U�ϑԂł��K���E�s�K���ϑԂł͌��q�ԋ������x��
�Z�����g�U�ŋK���i�q�̌`�����s����B
�@�َ�����̂Q���n�ŗn�̂͒ʏ�u���^�ŗn�̂ƂȂ邪���̒u���^�ŗn�͉̂��x��������ƋK���E�s�K��
�ϑԂ�����ꍇ�Ƒ��������N�����ꍇ������B
�@
�@�Q���n�ŗn�̂łَ͈팴�q�̕��z�͖������̏ꍇ�ƋK���z��ꍇ������B
�@���َ̈팴�q���K���I�ɔz���\�����K���i�q�Ƃ����A���̕ϑԂ��K���|�s�K���ϑԂƂ����B
�@�K���|�s�K���ϑԂ͌ŗL�̕ϑԓ_���������ϑԂ͏��X�ɐi�ށB
�@�K���i�q�̌`����X����܂̃T�C�h�s�[�N�̏o���Ƃ��Ċϑ������B
�@Ni�APd�APt�̑J�ڋ�����Cu�AAg�AAu�̋M�����œT�^�I�Ɍ�����B
�@�����͒ʏ�ʐS�\�������K�����ɂ͊i�q�̋��ƖʐS�ɂ��ꂼ��K��������A3B�iAB3�j�\����A��B��
���ꂼ��قȂ�ʂɂ��낤AB�\��������B
���������K���\����
�@CuAu������Cu���q�݂̖̂ʂ�Au���q�݂̖̂ʂ�C�������Ɍ��݂ɐϑw����CuAu�T�ƁACuAu�T�̒P�ʖE��
�����ɂT�����Ɉʑ������炵�ĕ���{�\����10�{�̒P�ʂ̍\���̒������\����CuAu�U�̂Q��ނ�
�K���\����������B
���t�ʑ����E�Ɣ��\�����@
�@���q�̋K���z��̈ʑ����H������Ăł����E�ʂ��t�i���j�ʑ����E�Ƃ����B�@
�@�������\���̎�������{�\���̐����{�ɂȂ�Ȃ��ꍇ�����肱������\��incommensurate�Ƃ����B
�i�V�|�Q�j�@���f�ϑԁ@
�@�g���ω��̂Ȃ������\���̕ω��B
�@��ʓI�ɂ͒ቷ���獂���ł̕ϑԂ͖ʐS�����A�f���Z�����̂悤���f���Ȍ��q�z�u����̐S��������
�悤�ȑa�ȍ\���ɕϑԂ���ꍇ�������B
�@�����œ��f�ϑԂ�����ꍇ�A�ቷ���烿�A���A���E�E�E�Ə̂���B
�@�e���ł̓��i�������j���X�P�Q���F���i�������j���P�R�X�S���F�i�������j�Ɠ��f�ϑԂ���B
�@�Ȃ����͌����\���̕ω��̐����Ȃ��d�q��Ԃ̕ω��ɂ�鎥�C�ϑԑ��ł���B
�@���̂ق��b���̓��i�������j�����i�������j�A�s���̓��i�������j�����i�������j�̓��f�ϑԂ��s���B
�@�r���̓����������̓��f�ϑԂ��s���A�퉷��������ቷ�����ւ̕ϑԂ��r���y�X�g�Ə̂���B
���z���w�ł͑g���������Ō����\���̈قȂ���̂��i�����j���`�Ƃ����A���Ɍ��f�z���̏ꍇ�f�̂ƌĂ�
���Ƃ�����B
�@���f�ϑԂȂ����͑��`�̑��ϑԂ̋@�\�����ƂȂ邪���`�ɂ��Ă͊g�U�ɂ����̂�����Ƃ�����B
�@���`�͔�r�I�ቷ�Ő������������葊�ł���ꍇ�������A�ő̓����]�ڂɑ��n�t�}��]�ڂɂ�����
���Ȃ킿�n�t���ł̗n���E�Č����̌��ʐ����鑊�]�ڂł���ƍl������B
�@����X�̗ގ��A�މ��I�����\��
�@�E�|���e�B�s�Y��polytiypism�ƃ|���^�C�vpolytype
�@�@�|�������t�B�Y��Polymorphism�i���`�j�̓���ȃ^�C�v�ŁA�����Q�����w�i�|���^�C�vPolytype�j�Őϑw�\�����قȂ錋���\���A
�@�_��A�S�y�A�l���r�Q�A�O���t�@�C�g�Ȃǂ̑w��\����r���b�Ō�����B
�@�@�|���e�B�s�Y�������������̐ςݏd�˂̊�b���Ȃ��X�̍\�����|���^�C�v�ƌĂԁB
�@�@�����|���^�C�v�̈قȂ�ϑw�\���ɂ��قȂ錋���\�����������̂��|���e�B�s�Y���B
�@�E�|���^�C�|�C�hpolytypoid
�@�@�z�C�I���^�A�C�I����ω��ɂ���Č`�������ϑw���ׂ̐���B
�@�@�\���������őg������قȂ�B
�@�@���������z�C�I���^�A�C�I�����}��Ƃ���g���Ɉˑ����錇�\���B
�@�@�r���R�m�S�|�`���Q�n�R�n�i�T�C�A�����j�ł͂U�̃|���^�C�|�C�h������\���͋����^�������A�l�^�w�Ō��肳��A
�@�l���w���|�P�ł����S����X��Ramsdell�L���łg�C�P�T�q�A�P�Q�g�A�Q�P�q�C�Q�V�q�A�Q�g�B
�@�@�|���e�B�s�Y���͑g���ω��̂Ȃ����\���A��r���b�B
�@�E�z���I�e�N�ghomeotect�@
�@�@�@Parthe�͓����w���x�����Ŏ������قȂ�\�����z���I�e�N�g�ƌĂB
�@�@�@�z���I�e�N�g�͋��ʒP�ʃX���u�i���j�̈قȂ�ςݏd�ˍ\���ł���B
�@�@�@�f���[�U�\���i�������A�������j�A�r���b�\���A���[�x�X���`�a�Q�A�W�V���P�[�g�i�l���r���Q�j�\���ȂǁB
�@�E�U�����t�B�Y���A�U���`pseudomorphism
�@�@���̍z���̊O�ς������z���ŁA�O�`���ێ����ꂽ�܂܂œ����\���A���w�g�����ω����邱�ƂŐ�������B
�@�E�����n��homologous series��
�@�@�J��Ԃ���铯��ςݏd�˂̑w���̈Ⴂ�ɂ���Č`�������P�A�̍\���B
�@�@VnO2n-1�̂悤�Ɋ�{�ƂȂ�\���P�ʂ�, ����̌��q�ʂ������������邢�͑}�����邢��, 2��ނ̊�{�\����ςݏd�˂��\��
�@���Ȃ钷�����\�������œ���̈�ʎ��Ƃ��ĕ\�������.�n��B
�@�@���ʍ\�������Œz���ꂽ�\���P�ʂ��Ȃ�A�������w�v�f���قȂ銄���Ŋ܂݁A�P�ʂ̑傫�����قȂ�B
�@�@�����{�\�����炠��Č��������ň����o���ꂽ��A�̌n��B
�@�@�|���]�}�e�B�b�Npolysomatic�iaccretional�j�����n���variable-fit �����n����B
�@a�D�|���]�}�e�B�Y��polysomatism
�@�@�@�Q�ȏ�̍\���P�ʁi���W���[���A�X���u�j�̑g�ݍ��킹�Ƃ��ĕ\������鑽�l�ȍ\�����ł��錻�ۂ��|���]�}�e�B�Y���ŁA
�@�@���̂悤�ɂ��ĕ\�������z�����|���]�[��polysome�A�z���Q���|���]�}�e�B�b�N�n��Ƃ����B
�@�@�@�\���P�ʂ�A, B�Ƃ���ƁiAB�j,�iABB�j,�iABA�j�c�Ȃǂ�����ɂ�����, �V�R�̍z���Q�ł̓q���[�}�C�g���z����biopyriboles�Ȃǂ�
�@�@�������, rutile�^��perovskite�^�̍\�����������ɑ��ēK�p�������̂�����B
�@�@
�@b�Dvariable-fit �����n��
�@�@�@�ЂƂ̍\���ɑ傫���̈قȂ�Q�̕��i�q������悤�ȍ\���B
�@�@�@�Q��ނ̌��݂���݂��ɔ��ȍ\���u���b�N�����n��B
�@�@�@�e�u���b�N�͂��ꂼ��̒Z�͈͎����������B
�@�@�@���u���b�N�̎n�_�������ɂȂ�܂ň���͂��ő����͂������B
�@�@�@������Semi-commensurate ���F�������ɑ傫���͂Ȃ������̂Ƃ�
�@�@�@��Incommensurate�@�@���F�������ɑ傫�������̂Ƃ�
�@�@

�@�@�@variable-fit �̖͎��}
�i�V�|�R�j�@���g�U�ϑ�
�i�V�|�R�|�P�j�@�}���e���T�C�g�ϑԁ@
�@�}���e���T�C�gmartensite�͒Y�f���܂ލ|�������i�I�[�X�e�i�C�g���j����Ă�����i�}��j�����Ƃ��Ɍ`��
�����Y�f���ߖO�a�������ɍd���g�D�ł���B
�@���̃}���e���T�C�g�ϑԂ͌��q���g�U�킸�ɋ����I�Ɉړ����邱�Ƃɂ���Đ�����ϑԂł���B
�@�ό`�͂���f�i������j�ɂ���ċN����A����f�ό`�ɂ͂��ׂ�ό`�i�S�̂����������ɂ����j�Ƒo���ό`
�i���݂̕����ɂ����j������A�\�ʌ`��̋N������������B
�@�܂��ꑊ�ƃ}���e���T�C�g���̊Ԃɂ͈��̌����w�I���ʊW���������̏��Ȗʂ����B
�@�}���e���T�C�g�ϑԂ͔�g�U�^�̑��ϑԈ�ʂɊg�傳���\�����]���ƌĂ��悤�ɂ��Ȃ�X�ɋ@�\�Ƃ���
�i�q�U���̓���̃��[�h�i�\�t�g�t�H�m���j�̓����ɂ����̂Ƃ����l��������������Ă���B
�@�}���e���T�C�g�ϑԂ͌`��L�����邢�͒��e���ƌ��т��Ă���ꍇ������B
�E�M�e���^�}���e���T�C�g
�@�ꑊ����}���e���T�C�g�ւ̕ϑԉ��x�ƃ}���e���T�C�g����ꑊ�ւ̕ϑԉ��x�̉��x���i���x�q�X�e���V�X�j���������A�ϑԂ̉t��������B�@
�@�M�e���^�}���e���T�C�g�ł͉��x���͂Q�O���ȉ��ł��邪�S�|�S�O�O���ȏ�B
�@�M�e���^�}���e���T�C�g�͂قƂ�NjK�������ł���A���ꂪ�ϑԂ̉t���������炷�ƍl������B
���o���A���gvariant�i�Z�푊�j
�@�o���A���g�Ƃ͌����\���͓����i�����w�I�ɓ����j���������w�I���ʊW�i�~�X�I���G���e�C�V�����F���ʊp�j�̈قȂ錋���h���C���i�̈�j�B
�@�S�|�̃}���e���T�C�g�iKurdjumov-Sachs(K-S)�W�j�ł͂Q�S���ʁi�Q�S�̃o���A���g�j�����݁B
�@�������̂̎���A���U�d�̂̕���A���e���́i�����Ђ��݂������O�͂Ŕ��]�j�̕�����o���A���g�Ƃ�����B
�@�m���Q�l���f���A�m���Q�e���f�����̃z�C�X���[�����͋������}���e���T�C�g�Ń}���e���T�C�g���o���A���g�Ǝ��悪��v����B
�E���e��
�@�M�e���^�}���e���T�C�g�ł͊O�͂ɂ������ėD������i�e���c�݃G�l���M�[���������j�����̃o���G���g����������B�@�@
�@�ꑊ����}�������T�C�g���ւ̕ϑԁi���͗U�N�}���e���T�C�g�j�A���邢�̓}���e���T�C�g�E�o���A���g�Ԃ̐H�������A�X�ɂ͕ʂ̃}���e���T�C�g��
�ւ̕ϑԂŌ��ʓI�ɑ傫�ȕό`���t�I�ɐ����錻�ۂ����e���B
�@�M�ɂ���ĕό`���t�I�Ɍ��ɖ߂錻�ۂ��`��L���B

�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@���͂ɂ��D������o���A���g�ւ̒P�ꉻ�̖͎��}
�E���́i���H�j�U�N�ϑ�
�@�}���e���T�C�g�ϑԂ��鍇�����}���e���T�C�g�ϑԉ��x�ȏ�̉��x�ʼn��͂�������ƃ}���e���T�C�g�ϑԂ��N�����B
�@���̉��͂������Ƃ��Ƃ̑��ɖ߂�B�i���e���j
�@�܂��}���e���T�C�g�͉��͂ɂ���č\���̈قȂ�}���e���T�C�g���i�o���A���g�A�������ʂ��قȂ�j�ɕϑԂ��邱�Ƃ�����B
�@���邢�̓}���e���T�C�g�ϑԂ��N�������Ă����ۂ̓I�[�X�e�i�C�g�������݂��i�c���I�[�X�e�i�C�g�j�A����ɉ��͂�
������ƃ}���e���T�C�g�ϑԂ��N�����B
�@���̎c���I�[�X�e�i�C�g�̃}���e���T�C�g�ϑԂ𗘗p�����̂��s�q�h�o�i�ϑԗU�N���Y���j�|�ł���B
�@�W���R�j�A�͉��͂ɂ���Đ���������P�Ώ��ւ̕ϑԂ��N���B
�i�V�|�R�|�Q�j �x�C�i�C�g�ϑ�
�@�S�|�����̉��x�ŕϑԁi�����܂��͍P���ϑԁj�������Ƃ����x�̍����ق�����p�[���C�g�A�x�C�i�C�g�A
�}���e���T�C�g�ƌĂ��ϑԂ��N�����B
�@�p�[���C�g�͏�q�̂悤�Ƀ�Fe�i�������j����Fe�i�������j�{Fe3C�@�̊g�U�ϑԂł���B
�@����}���e���T�C�g�͖��g�U�ϑԂł���B
�@���̒��Ԃł�����x�C�i�C�g�ϑԂ͔��ׂȃ�Fe�ƃZ�����^�C�gFe3C�̕����g�D�ł��邪�ϑԂ̋@�\�ɂ��Ă�
�����̉ߒ��Ŗ��g�U�ϑԂ��֗^����Ƃ�����Ȃǂ���͂����肵�Ă��Ȃ��B
�@
�@�@

�@�@�@�l���F�}���e���T�C�g�ϑԊJ�n���x�A�l���F�}���e���T�C�g�ϑԏI�����x�A�o���E�o���F�p�[���C�g�A�a���E�a���F�x�C�i�C�g
�@�@�@�@�@�@���͒Y�f�|�̂s�s�s�}�i�P���ϑԐ��}�A�I�[�X�e�i�C�g�̈悩��̋}��ł��鉷�x�ŕێ��j
�@
�i�V�|�R�|�R�j�@�}�b�V�umassive�ϑԁ@
�@�����n�Ō����\���̂ݕω����g���s�ς̕ϑԂŁA�E�ʂł̌��q�̒Z�͈͊g�U�ɂ��E�ʂ̋}���Ȉړ��ɂ��
���ϑԂƍl�����Ă���B
�@�j�������̕ꑊ�Ƃ͌����w�I���ʊW�������g�U�ɂ���ĕϑԂ��i�s���邽�ߓ���̏��Ȗ�
�i�͏o���₷�������ʁj�͂����Ȃ��̂Ń}�b�V�u���ɕϑԂ��Ă������̕ꑊ���Ƃ͌����w�I���ʊW�͂Ȃ��B
�@��Ƃ���Ti-Al��������������}�₵�ē��������������B
�i�V�|�R�|�S�j�@�֕ϑ�
�@���������i�s���A�y���Ȃǂ̂������j�ɂ悭�������]�ȉ~�̏�̐͏o���B
�@�R�w�����̂Q�A�R�w�ڂ̖ʂ��݂��ɋ߂Â��l�ɕψʁi�V���b�t���j�B
���r���y�X�g
�@���x�̍����r���͏퉷�ł̓��r���i�������F���x�V�D�Q�W�j�ƂȂ��Ă��邪�ቷ�i�]�ډ��x�͂P�R�D�Q���Ł[�R�O����
�]�ڑ��x�̋ɒl���Ƃ�Ƃ�������j�Ń��r���i�_�C�������h�����F���x�T�D�W�j�ɓ��f�ϑԂ���B
�@���̕ϑԂ͂Q�U���̑̐ϑ������������ɖc�����A����������B
�@�X�ɂ��̕ϑԂ̓��r���ɐڐG������Ƒ��i�����i���ȐG�}�I�j�B�i�`������I�y�X�g�Ƃ������̗R���j
�@
 �@�r���|�O�D�T���b�����Q�T�T�j�łP�D�T�N�u�����Ƃ��A�i���J����̕����j
�@�r���|�O�D�T���b�����Q�T�T�j�łP�D�T�N�u�����Ƃ��A�i���J����̕����j��Cohen�AOlson�AClapp�͖��g�U�ϑԂ����̂悤�����������B
�@�@�EShuffle�ϑԁ@�s���A�y�������i�����ցj�A�r���s���n�R�A�j�g�Q�o�n�S�ȂǁB
�@�@�E�i�q�ό`�ϑԁ@
�@�@�@�@�E�L�k�x�z�@�@�@�r���i�������j
�@�@�@�@�E����f�x�z�@�@
�@�@�@�@�@�@�@�E�}���e���T�C�g
�@�@�@�@�@�@�@�E���}���e���T�C�g�@�@�l���|�m��
�i�V�|�S�j�@�A�����t�@�X�����Ƌ����K���X�y�я������@�@
�i�V�|�S�|�P�j�@�A�����t�@�X����
�@�A�����t�@�X�Ƃ͂w����܂Ō������L�̉s���s�[�N�����������L���s�[�N�i�n���[�j�������̂ł���B
�@�����̓A�����t�@�X�ɂȂ�ɂ������t�̋}��@�ŋ����̃A�����t�@�X�����\�ł���B
�@�����ł͂r���A�f���A�o�A�b�A�o��������ƃA�����t�@�X�����₷���B
�@�A�����t�@�X�����ɂ͉��M�ɂ��K���X�]�ډ��x�ɒB����܂��Ɍ��������i�s���K���X�]�ړ_
�������I�Ɋώ@���邱�Ƃ��o���Ȃ����̂������B
�@�A�����t�@�X�����͗��E�A�͏o���⌇�ׂ��Ȃ����ߍ����x�i�������苭�x�A�Ⴤ���O���j�A����A�ϐH��
�Ƃ��������������A�e���ό`�̂��ƑY���ό`�Ȃ��ɔj��B
�i�V�|�S�|�Q�j�@�����K���X
�@�}��ɂ��Ȃ��ł��A�����t�@�X�������������������K���X�ƌĂ��B
�@�����K���X�͌���������O�ɃK���X�]�ډ��x�s�������A�����t�@�X�ł���B
�@�����^�������x�̗�p���x�ł��K���X�����o���N�̋����K���X��������B
�@����������O�ɃK���X�]�ډ��x�s�����������������x�s���Ƃs���̊Ԃ̉ߗ�p�t�̏�Ԃ�
�S��������ԁi���Y���j�������B
�@�����I�ɂ͂R���f�ȏ�̑����n�A�e���q�̌a���P�Q���ȏ�قȂ�A�e���f�������������₷��
�Ƃ����X�������Ƃ�����B�i��㖾�v���̂R�����j
�@�o���n�ōŏ��Ɍ��o����y���n���ŏ��Ɏ��p�����ꂽ�B
�@Zr55Ni5Al10Cu30 ����\�I�B
�@�@�@�@�@
�i�V�|�S�|�R�j�@������
�@�������͌�����A�����t�@�X�Ƃ��قȂ�ő̕����̍\���ł���B
�@��܃p�^�[�������I�A�t�i�q�_���L�q�����{�x�N�g������������葽���K�v�A�ʏ�̌����\��
�ɋ�����Ȃ���]�Ώ̐���L���Ƃ������������B
�@�����͕��i�Ώ̐���L���A���̉�]�Ώ̐���2��A3��A4���6��Ɍ����Ă��邪�A�����̏�������
��20�ʑ̍\��������5��Ώ̐���L����B
�@����\�ʑ̑��͊�{�\���ƂȂ�N���X�^�[�\���ɂ��AMI�^�i�}�b�J�C��\�ʑ̌^�j�ART�^�i�H�`�O�\�ʑ̌^�j
�ɕ�������B
�@���̑����W�p�`�A���P�O�p�`�A���P�Q�p�`�������o����Ă���B
�@�����͏������ʂɐ����ȕ����͎����I�ɐϑw�����\����L������������ł���B
�@���q���K���I�ɔz�Ȃ�����A�ʏ�̌����̂悤�Ȏ����I�\���͎������A�P��̒P�ʖE�ŋ�Ԃ�������
���o���Ȃ��B�i�t�i�q�_���L�q�����{�x�N�g������������葽���K�v�j
�@�Ƃ��A�d�C��M���`���ɂ����Ȃǂ̓��������B
�@�������͔M�I�ɕs����Ȃ��̂������AAl-Cu-Fe��Mg-Al-Cu�Ȃǂ̂悤�ɁA�R�ȏ�̌��f����\��������
����ɂȂ�X��������B
�@�������͎�ɉt�̋}��@�ɂ��쐬����A���J�j�J���A���C���O�@�ł͕�����������B
�@�t�F�C�]���Ƃ������L�̋Ǐ��I�ȔM��炬���ۂ������B
�@�������Ɠ����Ǐ��\����L���錋����������ߎ������Ƃ����B
�@�����͂�������U������Ԃ̎����\���ɂ�肻�̍\�������������B
�i�V�|�T�j�@�ŗn�̂Ƌ����ԉ�����
�i�V�|�T�|�P�j�@�ŗn��
�@�ŗn�َ͈̂팴�q�����q���x���ō����肠������ԂŁA�����̑��Ƒg�D�͂`�a�Q���n�ɂ��Ă݂�Ƃ܂�
���ׂĂ̑g���Ŋ��S�Ɍ��q���x���ō����肠���S���ŗn�̂��l�����b���|�m���n�Ȃǂ�����B
�@�ŗn�̂ň��̗Z�_�ŋɏ��l�������̂�����B�i��Z�_����congruently melting alloy�j
�@�@
 �@
�@

�@���̋t�Ɍ��q���x���ł��܂荬���肠��Ȃ��ꍇ�͋����ƂȂ�r���|�o���Ȃǂ̗Ⴊ����B
�@��ʓI�ɂ͍����ʂ����Ȃ��g���ł͌ŗn�̂ƂȂ�ꍇ������������ꎟ�i���j�ŗn�̂Ƃ�т₪�Ē��ԑ�
�i���j���`�����A���ŗn�̂ƃ����̊Ԃ́i���{���j�̂Q���g�D���`������̂���ʓI�ł���B
�@�����珇�ɐ����鑊�����A���E�E�Ə̂��邪���ȊO�͂قƂ�Nj����ԉ������ł���B
�@���������f�ϑԂ̂�����̂͒ቷ�����烿�A���A���E�E�E�Ə̂���B
�@
�@�ŗn�͉̂��x�ɂ���Čŗn�ʂ��ω��i�n��x�Ȑ��ƌŗn���A���x��������ɂ�Čŗn�ʂ������j���A
���̂��߉ߖO�a����̐͏o�i�����j���N����ꍇ�������B
�@�܂��ŗn�̂ɂ͖������ɍ����肠���s�K���^�ƋK���I�ɍ����肠���K���^������A���x��������ɂ�ĕs�K���^
����K���^�ւ̕ϑԂ��N�����������B
�@�܂����q�ʒu��u������u���^�ƌ��q���a���������ꍇ�͊i�q�ԂɐN������N���^������B
�@�ŗn�̂ɂ̓q���[���E���U���[�̖@��������B
�@�@�E���q���@���q�F���q���a�����P�T���ȓ��̂Ƃ��ŗn�����傫���B
�@�@�E���d�q�Z�x�i�P���q������̉��d�q�A�����ł͑g���ň��j�����̂Ƃ���Ɍŗn�����o���B
�@�@�E�d�C�A���x���q�i�d�C���w�I���q�j�F�d�C�A���x�i���d�q���j�̍����傫���قnjŗn�����������B
�@�@�E���Ό��q�����q�F�ጴ�q�������ɑ��鍂���q�������̈ꎟ�ŗn���͍����q�������ɑ���ጴ�q��������
�@�@�ꎟ�ŗn�����傫���B
�@�@�E�����\���������ƌŗn�̂��`�����₷���B
���e�퍇����
�@�N���^�����E�E�E�����ƐN���^�������`�����錳�f�͌��q���a�̏����Ȕ���������ł���B
�@�@�N���^�ŗn�́i�s�K���^�j�E�E�E�g�A�i�a�A�j�b�A�m�Ȃǂƌ`���A�}���e���T�C�g�i�b�j�A���f�z�������ȂǁB
�@�@�N���^�������i�K���^�j�E�E�E���f���������A�Y�����A�������ȂǁB
�@�@�@�@�@�@���Z�_�����̒Y�����A�������͓��d��������
�@�u���^����
�@�@�s�K���u���^���ŗn�́E�E�E�b���|�`�R�O�y���ȂǁA�ŗn����
�@�@�K���u���^
�@�@�@�@�����ԉ������E�E�E�`���|�b���A�`���|�l�����W�������~���̊�b�n�B
�@�@�@�@�K�������i�K���i�q�j�E�E�E�K���E�s�K���ϑԂ��s�����̂̋K�����i�ቷ���j�A�M�e���}���e���T�C�g�ƂȂ���̂������B
�@�@�@�@�@�M�������������E�E�E�E�b���|�`���i���ȗp�����̊�b�j�A���b���y���A�`���b��
�@�@�@�@�@�e���|�o���i�M�����j�E�E�E�M������������
�@�@�@�@�@�z�C�X���[�����E�E�E�P�̌��f�ł͋����������������Ȃ����̂��������ŋ������̂ƂȂ�B
�@�@�@�@�@�@�t���E�z�C�X���[�����E�E�E�w�Q�x�y
�@�@�@�@�@�@�n�[�t�E�z�C�X���[�����E�E�E�w�x�y
�@�@�@�@�@�@�@�w���J�ڋ����i�W�A�X�A�P�O�A�P�P���j�A�x���l���A�y�����u���b�N�T�^���f�i�h���A�r���A�f���A�f���A�r���A�r���j
�@�X�s�m�[�_���ϑԍ���
�@�@�@�e���|�b���i���邢�͍��Z�_�����j
�@�@�@�@�@���b���|�i�t�F���C�g���j�̂S�V�T���Ɖ��A�b���̍���Q���ɃX�s�m�[�_���ϑ�
�@�@�@�X�s�m�[�_������
�@�@�@�@�@�b���|�m���|�e���A�e���|�m���|�`���i�|�b���j�A�e���|�b���|�b��j����
�@�@�@�X�s�m�[�_���b������
�@�@�@�@�@�b���|�m���|�r���A�b���|�s��
�i�V�|�T�|�Q�j�@�S���ŗn�����̎�X�̌^
�@�@�A���J�������ԁA�A���J���y�ދ����ԁA�M���������ԁA���Z�_�����Ԃł͑S���ŗn�������`������₷���B
�@�@���̂ق��f���|�r���A�r���|�s���A�a���|�r���ȂǁB
�EIsomorphous���`�u��
�@�@�@�������\���������Ō��q���a���߂����f���u�B
�@�@�@�@�`���|�o���@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�`���|�`���@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�l���|�v
�@


 �@
�@�@�@
�@�@�@�@�b���|�m��
�@

�@�@�`���|�o���A�`���|�o���A�`���|�`���A�b���|�m���A�b���|�v�A�b���|�o���A�b���|�o���A�m���|�q���A�l���|�v�A�l���|�u�A�l���|�s���A�l���|�v�A
�@�@�l���|�m���A�h���|�o���A�h���|�q���A�u�|�v�A�t�|�y���A�s���|�v�A�s���|�s���A�s���|�v�A�s���|�t�A�l���|�s���A�s���|�s���A�r���|�y���A�m���|�v�A�m���|�t�A
�@�@�m���|�s���A�m���|�s���A�g���|�y���A�g���|�r���A�g���|�t�A�a���|�r���A�a���|�r���A�f���|�r���A�r���|�s���ȂǁB
�@
�E��v�]��congruent transformation�^
�@�@�@�@�ő����Ɖt�����̈�v(��v�n�Z�A��v�]��)
�@�@�@�@�ɒl������
�@�@�ɏ��l�^�i���ᑽ���j�@�@�@�@�@�@�@�@�@�@�@�@�m���|�o��
�@�@
 �@
�@ �@�@�@�@�@�@�@�@�@�@�@�@
�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@
�@�@�@�`���|�b���A�`���|�m���A�b���|�o���A�b���|�o���A�b���|�l���A�b���|�u�A�b���|�s���A�b���|�j�A�b���|�q���A�j�|�q���A�m���O�o���A�m���|�o���A�s���|�y���A
�@�@�s���|�y���A�s���|�y���A�s���|�u�A�b���|�s���A�r���|�s���A�r���|�s���A�m���|�y���A�m���|�u�A�g���|�s���A�g���|�s���A�a���|�b���A�b���|�r���ȂǁB
�@�@�ɑ�l�^�i���݂����H�j�@�@�@�@�@�@�@�@�@�@
�@�@

�@�@�@���̃^�C�v�̗�ɂl���|�k���A�o���|�s�����������Ă��邪�A�������邢�͕Ώ��̂悤�Ɍ�����B
�@�@�@�@�l���|�k���@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�o���|�s��
�@
 �@
�@
�@�@�@�@�@�@�@�@�@
�@�@�P���ω��^�i���݂����H�j
�@�@

�@�@�ŗn�x�M���b�v�^�A�Q�������^
�@�@�@���q���a�����傫���Ȃ�ƌŗn�x�M���b�v�ƂQ��������������B
�@�@�@
�@�@
 �@�@�@
�@�@�@
�@�@�@�@�`���|�m���@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�b���|�l��
�@
 �@
�@
�@�@�@�@�`���|�o���@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�b���|�v
�@


�@�@�@�K���]�ڌ^
�@�@�@�@�b���|�o���@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�m���|�o��
�@


�@�@�@���ԑ��^
�@�@�@�@�e���|�u�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�b���|�e���i�X�s�m�[�_�������j
�@


�@�@�@���f�ϑԌ^
�@�@�@�@�s���|�g���@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�y���|�g��
�@


�@�@�@�����ւ̈ڍs
�@

�@�@�@��ւ̈ڍs�i�Z�_�����傫���ꍇ�j
�@

����v�n�Z�ƃM�b�u�XGibbs�E�R�m���@�H�tKonovalov��
�@�@�Q�������Ȑ��̌X����
�@�@

�@�@�@�@�@�f��������
�@�@���邢��
�@�@�@

�@�@��v�n�Z�_�ł͂w���`�|�w���`���O������i�f���������L���ŕ��ꂪ�O�łȂ���j���Ӂ��O�ƂȂ�
�@�X���O�ŋɒl���ϋɓ_�ƂȂ�B
�i�V�|�T�|�R�j�@�����ԉ�����
�@�����̒��ԑ��ɂ͈��̑g���Ŕ�����I�����i�����l�����e���j�������G�Ȍ����\���̍d���āA�Ƃ�
�����ԉ������ƌĂ�鑊���`������邱�Ƃ������B
�@�����͒ʏ퍇�����ɂ���ėZ�_�������邪�A�����ԉ��������`������ƗZ�_���㏸����B
�@��Ԑ}�ł̏o���l������ȉ���3�^�C�v��������B
�@Kurnakov�^�F�����ł͕s�K���ŗn�̂Œቷ�ŋK�������`���A�b���R�`���A�b���`���A�e���R�`���A�s���R�`���ȂǁB
�@Berthollide�^�F����g�����������Ȃ��瓯�ꌋ���\�����Ƃ���́B
�@Daltonide�^�F�g���ɕ����Ȃ��B�\�����f�̐����̈Ⴂ���傫���ꍇ�������B
�@����ʓI�ɕs��䉻�����A�w�ʘ_�I���������x���g���C�h�A��䉻�������_���g�i�C�h�B
�@�����ԉ������͌����l���⌋���\�����番�ނ����݂���\�I�Ȃ��͈̂ȉ��̂悤�Ȃ��ł���B
�@�E�d�q�������F���d�q�Z�x�����̂Ƃ���ɓ���̌����\���̋����ԉ��������o���B
�@�@�@�R�^�Q�F�����Z�V�E���^�\���A����
�@�@�@�Q�P�^�P�R�F�b���T�y���W�^�\���A����
�@�@�@�V�^�S�F�b���y���R�^�\���A��
�@�E���q���a�������Fsize factor compounds�@���s�b�o���itopologically�@close-packed�j
�@�@�@���[�x�X���`�a�Q�F���q���a�䂪��P�D�Q�i1.225�F1�j�̂`�a�Q�^��
�@�@�@�@�@�@�l���b���Q�^�\���A�l���y���Q�^�\���A�l���m���Q�^�\���E�E�E
�@�@�@�Б��iFrank-Kasper���j�FFeCr����{�Ƃ�������ԉ������B1���q��30���q���琬��B
�@�@�@�@�@�@�������J�ڋ����ԂɌ�����A�d���ĐƂ��B
�@�@�@�@�@�@�j�����ɂ��N���蒷���Ԃ̍����ێ����K�v�B�m���������X�e�����X�|�B
�@�@�@���̑��ގ��̂��̂ɃA�ʁA�ԑ��E�E�E
�@�@�@�N���^�������@
�@�@�@�@�@�������q�Ƃg�A�m�A�b�E�E�E
�@�E���q�����ʉ�����normal valency compounds
�@�@�@�C�I�������^�C�v�@�i�d�C���w�I������electrochemical compounds�j
�@�@�@�@�m���b���^�\���A�b���e�Q�^�\���A�t�b���e�Q�^�\���A�E�E�E
�@�@�@���L�����^�C�v
�@�@�@�@�y���r�^�\���A�E���c�@�C�g�^�\���A�m���`���^�\���E�E�E
�@���`�P�T�i���^���O�X�e���\���j
�@�@�@�@�@�`�R�a�A�`�͂b���A�l���A�m���A�s���A�u�A�y���ȂǁA�a�͂f���A�f���A�h���A�q���A�r���A�`���A�r���A�r��
�@�@�@�@�@���`���������B
�@��Zintl���i�W���g�����j
�@�@�@�@�@�A���J���܂��̓A���J���y�ދ����i�`�j�ƂP�R����P�U���̓T�^���f�i�a�j�Ƃ̉������B
�@�@�@�@�@�a���q�����L�����ŃN���X�^�[�A�w��A�Ԗڏ�\�����`������ۂɃI�N�e�b�g������s������d�q���`���q����
�@�@�@�@�₤�B
�@���m�{�g�j�[���˒�qNowotny Chimney Ladder��
�@�@�@�S����X���J�ڋ����s�i�l���A�q���A�h���A�u�A�b���A�l���A�q���E�E�E�j�ƂP�R�A�P�S�A�P�T���T�^�����d�i�`���A�f���A�r���A�f���A�r���E�E�E�j
�@�@�ɂ���Č`�����������ԉ������s���d���B
�@�@�@�Q�̌o����
�@�@�@�@�J�ڋ�������̉��d�q�����P�S�B
�@�@�@�@��܃X�|�b�g�͎唽�˂̎���ɃT�e���C�g�i�����ˁj�����B
�@�@�@�@�@�唽��c���̎���ɋU������cpseudo�̑��݁A(2t-m)��c=c��pseudo
�@�@�@�@�@�唽�˂����̑��ɕ�������cpseudo�̑���
�@�@�@�@�@����Ԃł�(2t-m)cpseudo=c
�@�@�@�@�@������(2t-m)��cpseudo���J��Ԃ��B
�@�@�@�P�ʖE�͂����ɉ����Ăs���q�̂��̋U�Z���Ƃd���q�̂��̑��ݐN������U�Z���������Ă���B
�@�@�@�J�ڋ����̂S��点��\��������chimney�A�T�^�����̕ʂ̂点��\������qladder���`���B
�@�@�@�q���f���Q�ł͂q�����˂̂点��̎��͂ɂf����q���Q��点����`���B
�@�@�@�q���Q�r���R�ł͂r���点��̎�����q���̂R��点�͂ށB
�@�E�f�b�o���igeometrically close packed�j�@
�@�@�@���ʂ̍Ŗ��ʁiFCC�AHCP�|common close-packed plane CCP�j�̎����I�Ȑϑw�ɂ�钷�����\�������B
�@�@�@�@Ni3X �^�������ł͐ϑw�����\���E�E����ϑw�ɋ��܂ꂽhexagonal-layer(AB)�ƁA�َ�ϑw�ɋ��܂ꂽcubic-layer
�@�@�@(ABC)�ƍŖ��ʏ��X ���q�z��E�ETriangle-type(T) ��Rectangle-type(R)�ɂ���ē����t������B
�@���f�b�o�ُ̈틭������
�@�@��ʓI�ɋ����̍~�����͉͂��x�̏㏸�ɔ����A���X�ɒቺ���邪�A�ꕔ�̂f�b�o�����ԉ������ł́A
�@���鉷�x�͈͂ʼn��x�̏㏸�ɔ������x���㏸����ُ틭�����ۂ�������B
�@�@��Ƃ��Ăk�P�Q�i�m���R�`���j�A�c�Oa�i�m���R�m�� Bertholide�^�j�A�c�O�P�X�i�m���R�r�� Kurnakov�^�j�A�c�O�Q�Q�i�`���R�s���j�A�c�O�Q�R�i�`���R�y���j�A
�@�c�O�Q�S�i�m���R�s�� Daltonide�^�j�Ȃǂ�����B�@�����̌����\���\����Structurbericht�ɂ��B�@Structurbericht Designation ���c�^�@
�@

�@�@�@�ُ틭���i���x�̐��̉��x�ˑ����j
�@�@����͋K���i�q�̓]�ʂ��傷�ׂ�ʂ̂ق��ɔׂ�ʂɂ��ꕔ��������������ׂ���`�������ق���
�@���ʑ����E�`�o�a�G�l���M�[���������Ȃ邱�Ƃɂ��������ׂ�̌`���ɂ��Ƃ���Kear-Wilsdorf�@�\�i���b�Nlock�j��
�@�����������B
�@�@�@
�@�E�s�b�o���itopologically�@close-packed�j�@
�@�@�@���̑��̃Z���i�P�ʖE�j�\���͑��ΓI�ɑ傫�Ȍ��q�ԋ����ŕ������ꂽ�w�ɑ��݂����f�����q�����B
�@�@�@�m����b���̂悤�ȑ��ΓI�ɏ����Ȍ��q���f���w�Ƃ��̑w�Ԃ̂P�S�A�P�T�A�P�U���z�ʃT�C�g�ɂ���v�C�s���̂悤�Ȃ��
�@�@�傫�Ȍ��q���Ȃ�B
�@�@�@�S�ʑ́iFrank-Kasper �^�C�v�j�̒��S�ɂ��邱���̃T�C�g�̐����s�b�o��������t���A�L���͈͂̑g���Œu����������B
�@�@�@�f�����q�w�͂v�C�s���̂悤�Ȃ��傫�Ȍ��q�ɂ���ċ��܂�T���h�C�b�`�\�����Ƃ�A�g�|���W�J���i�ʒu�W�I�j�ȓ����������B
�@�@�@����ɑ��f�b�o�͂��ׂĂ̕������f���ł���B
�@�@�@�s�b�o�͒ʏ��`����Ƃ�B
�@�@�@�X�e�����X�|�ɐ�����TCP�̓ЁA�ԁALaves�AG�AR�A�ʂȂǂ�GCP�̓��f�A���h���ł���B
�@�@

�@�@�@�@�@�@�@�@�@�s�b�o���\����
�@��Frank-Kasper���itetrahedrally closed-packed (TCP)�j
�@�@���̏[�U����b�ɎO�p�z�ʊk�̊T�O�ŕ��G�����ށB�S�ʑ̍Ŗ��[�UTCP�Ŕz�ʐ��P�Q�A�P�S�A�P�T�A�P�U��������B
�@�i�����傫���̌��q�ɂ��Ŗ��[�U�͂S�ʑ̂ƂU�ʑ̋����݂���j
�@�@������TCP�̂S�ʑ̂͂��ׂĂ͋K���I�ł͂Ȃ��i���Disclination�����j�A�Ȃ��Ȃ�K���I�S�ʑ̂Ŋ��S�ɋ�Ԃ��݂������Ƃ͂ł��Ȃ��B
�@�@CN12�@�c�Q�O�ʑ́A�Q�O�̎O�p�`�ʂ��`���A���S���q�͂Q�O�̂S�ʑ̂ň͂܂��B
�@�@CN14�ACN15�ACN�P�U�͂��ꂼ��Q�S�ʁA�Q�U�ʁA�Q�W�ʁB�T�Œ��p�͂��ׂāiCN�P�Q���j�P�Q�łU�Œ��p�͂Q�A�R�A�S�iCN12�͂O�j�ł���B
�i�V�|�T�|�S�j���^���C�hMetalloid�A������Semimetal�ƃn�[�t���^��
�@�@���^���C�h�͉��w�I��������̕��ނŎ������\��ŋ����Ɣ�����̒��Ԃɂ�����̂ła�A�r���A�f���A�`���A�r���A�s���ȂǁB
�@�@������Semimetal�̓o���h�ō\���œ`���тƉ��d�q�т��G�l���M�[�I�ɏd�Ȃ��Ă͂��邪����Ԃł͗���Ă�����̂ŁA
�@�`���A�r���A�a����g���s���ȂǁB
�@�@�n�[�t���^���̓o���h�\���ŕЕ��̓d�q�X�s���������I�ŁA��������̓d�q�X�s���������̓I�Ȃ��́B���̂悤�ȃn�[�t�l�^����
�@�t�F���~�ʂŃX�s�����Ј�������ɂȂ��Ă���A�܂�X�s���ɂ��Ă��邱�ƂɂȂ�B�o���h�v�Z���z�C�X���[�����Ȃǂ��n�[�t
�@���^���̉\��������Ƃ����B
�@�@�z�C�X���[�����̓R�o���g�iCo�j�A�S�iFe�j�A�V���R���iSi�j�A���iCu�j�E�}���K���iMn�j�E�A���~�j�E���iAl�j�Ȃǂ̌��f���K������������
�@���Ԃ��Ƃŋ������̂ƂȂ�R���n�����ŁACo2MnSi�ACo2FeSi��Cu2MnAl�Ȃǂ�����B
�@�@���o���h�\���ɂ�镨���̕���
�i�V�|�T�|�T�j�����̗Z�_�@�E�E�E��Z�_����
�@�@�ቷ�͂A���x�q���[�Y�A�s���[�^�[�i����߁E�E�ቷSn�����A�H�|�p�����ޗ��j�ȂǂɎg�p�����Sn�𒆐S�Ƃ��鋤���n��
�@��Z�_�����i�Z�����A�Z�����j������B�iCs�ARb�AHg�Ȃǂ̈�������̂������j
�@�@��Z�_�����Ɏg�p����������Sn�APb�ACd�AIn�ABi�AZn�AGa�i�Z�_�R�O���j�Ȃǂł��邪�L�Q������Cd�APb��������BIn�AGa�͍����B
�@�@�퉷�t�̂�Ga-21.5In-16.0Sn�R�������͂P�O�D�V���AGa-21.5In-1�O.0Sn�i�K�����X�^���j�́|�P�X���Ƃ��B
�@�@��Ȓ�Z�_�Q��������Sn-�WZn�F�P�X�X���ASn-38Pb�F�P�W�R���i����Pb�͂j�ABi-42Sn�F�P�R�W���AIn-48Sn�F�P�P�V���A
�@B��-�R�RIn�F�P�P�O���AIn-34Bi�F�V�Q���AGa-24.5In�F�P�T�D�V���ȂǁB
�@���Z�_�ȏ�i�ő����j�ȏ�ŕ������Z����̂��o�Z�E�Z��melt�A�Z�_�ȉ��Ōő̕������n�}�ɗn����̂͗n��dissolve�B
�@�@�r���i�Z�_�Q�R�Q���j�Ȃ����r���͂ɍ��Z�_�̂`���i�Z�_�P�O�U�S���j�A�`���i�X�U�Q���j�A�b���i�P�O�W�R���j���ǂ��n�����邱�Ƃ��m���Ă���B
�@�@�n���ɂ��Ă�Nernst-Brunner�̎�dn/dt=KA/V�(ns-n)�An=ns�k1-exp{-K(A/V)t}�l����������B
�@�@�@�@n�Ft�b��̗n���Z�x�Ans�F�n���̖O�a�Z�x�AK�F�n���̑��x�萔�A,A�F�����ʐρAV�F�����t���̑̐�
�i�V�|�T�|�U�j�ő�����
�@�@�r���Ƌ����ԉ��������`����������i�`���A�`���A�o���A�b���A�m���A�e���A�b���A�o���E�E�E�j�̑����͌ő������ŋ����ԉ��������`������B
�@�@���ɂ`���Ƃb���͂͂Ƃ̊W�ŗǂ����ׂ��Ă���A�`���ɂ��Ă����C���{���f�B���O���ł悭�m���Ă���B
�@�@�g�U���邢�͂߂�����o�u�c�Őϑw�\���ɂ���ƁA�r���Ƃb���ł͌ő������łr������������b���U�r���T�A�����b���R�r�����`������A
�@�r���Ƃ`���ł͂r������������`���r���S�A�����`���r���Q�A�`���r�����`������邱�Ƃ��m���Ă���B
�@�@�`���ւ̂`�����C���{���f�B���O�ł͂`��������`���`���Q�A�i�`���`���j�A�`���Q�`���A�`���T�`���Q�A�`���S�`�����`�������Ƃ����B
�@�@�ő������ł͑����̏ꍇ�AKirkendall�{�C�h���`�������Ƃ������_������B
�i�V�|�U�j���ϑԁi���]�ځj�̑��i�Ɨ}��
�i�V�|�U�|�P�j�X�e�����X�|�̎��
�@�e���͍������Ƃ��Ă������̃����i�I�[�X�e�i�C�g�j�ƒቷ���Ƃ��Ă������̃����i�t�F���C�g�j�������A�X�Ƀ�������̋}��ł̓}���e���T�C�g��
���邱�Ƃ�����B�������̃I�[�X�e�i�C�g���������ŏ퉷�ň��艻���邱�Ƃ�����B
�@�X�e�����X�|�ɂ͂����R������������B
�@�b���n�X�e�����X�|
�@�@�@�t�F���C�g�n�X�e�����X
�@�@�@�@�@�@�t�F���C�g���i�̐S�������������j�A�P�V���b������{�i�r�t�r�S�R�O�j�B
�@�@�@�}���e���T�C�g�n�X�e�����X
�@�@�@�@�@�@�P�R�b������́i�r�t�r�S�P�O�j�B
�@�b���|�m���n�e�����X�|
�@�@�@�I�[�X�e�i�C�g�n�X�e�����X
�@�@�@�@�@�@�ʐS�������������A�ϐH���ǁA�P�W�b���|�W�m������{�i�r�t�r�R�O�S�j�B
�@�@�@�@�@�@�I�[�X�e�i�C�g���͔������P�W�b�|�W�m���͉��͗U�N�}���e���T�C�g�ɂ�莥����������̂łm���𑝂₵�āi�P�P�`�P�R���j
�@�@�@�@�@�I�[�X�e�i�C�g�������艻�B�@�@�����X�e�����X�i�r�t�r�R�O�T�j
�@�@�@�Q���X�e�����X
�@�@�@�@�I�[�X�e�i�C�g���ƃt�F���C�g�����Ȃ�A�t�F���C�g���艻���f�̂b�����I�[�X�e�i�C�g�n��葽���A�b���^�m�����I�[�X�e�i�C�g�n���傫���B
�@�͏o�d���n�X�e�����X
�@�@�@�����ԉ������ɂ��͏o�d���A�r�t�r�U�R�P�͂P�W�b���|�W�m���̐͏o�d���^�ő��ԉ������m���`�����͏o�B
�i�V�|�U�|�Q�j�S�|�ւ̍��������̌���
�E�t�F���C�g���艻���f�ƃI�[�X�e�i�C�g���艻���f
�@�@�t�F���C�g�i�����j�����艻���錳�f�i�t�F���C�g���艻���f�j�ɂ͂b���A�v�A�l���A�u�A�r���Ȃǂ�����B
�@�@�����̓�����胿���Ɍŗn���₷���A�����i�r����O�j�͂������\�������B�����̓����̂b�ʂ�����������B
�@�@�I�[�X�e�i�C�g�i�����j�����艻���錳�f�i�I�[�X�e�i�C�g���艻���f�j�ɂ͂l���A�m���A�b���A�b���Ȃǂ�����B
�@

�@�@�@�������艻���f�i�`�R�ϑԉ��x�ቺ�j�@���F����J���^�i�l���A�m���j�@�@���F����g��^�i�b�A�m�A�b���j
�@�@�@�������艻���f�i�`�R�ϑԉ��x�㏸�j�@���F�����[�v�^�i�r���A�b���A�l���A�`���A�s���A�u�A�v�j�@�@���F����k���^�i�m���A�y���j
�@�@�@�@�@�e���|�l�Q���n��Ԑ}�̕���
�@

�@�@�@�@�@�@�@�@�e���|�m���n��Ԑ}
�@

�@�@�@�@�@�@�@�b���|�e���n��Ԑ}

�@�@�@�@�@�@�e���|�b���n��Ԑ}
�@

�@�@�@�@�@�e���|�y���n��Ԑ}
�@

�@�@�@�@�@��X�̂e���|�l�Q���n�ł̃����[�v�̌`��
�@

�@�@�@�I�[�X�e�i�C�g�X�e�����X�|�ւ̍��������̌ŗn��������

�@�@�@�@�@�@�t�F���C�g���̌ŗn����
���n�ڂ̕���ł͗n�ڋ����̑g�D��m����@�Ƃ��ăt�F���C�g���艻���f�����艻�̒��x���b���ʂɊ��Z�����b�����ʂ������A�I�[�X�e�i�C�g
���艻���f���m�����ʂƂ��ďc���ɂ��g�D��\�����g�D�}���悭���p����A�V�F�t��Schaeffler�A�f�E�����ODe Long�A�v�q�b�i�č��n�ڌ����ψ���j��
�g�D�}���悭���p�����B�f�E�����O�̐}�ł͂m������ �� 30��C�{0.5��Mn�{��Ni�{30��N�@�Ƃm���܂܂�A�v�q�b�}�ł�Cr���ʁ���Cr�{��Mo�{
0.�V�~��Nb�ŕ\�����B
�@�@
�@�@

�E�Y�����f�̍P���ϑԂւ̉e��
�@�@���ʂȒY�������`�������t�F���C�g�ƃZ�����^�C�g�Ɍŗn���錳�f�͂b�����ϑԂ𑣐i����ȊO�m���A�r���A�b���A�`�����͕ϑԂ�}������B
�@�@�Y�����`�����f�i�b���A�l���A�v�A�u���j�͍P���ϑԂł̃I�[�X�e�i�C�g����̕ϑԂŁA�V�O�O�|�T�O�O���i�p�[���C�g�`���j�ł͕ϑԂ�}�����A
�@�T�O�O�|�S�O�O���ł͌��I�ɕϑԂ�}�����A�S�O�O�|�R�O�O���i�x�C�i�C�g�`���j�ł͕ϑԂ𑣐i����B
�@

�@�@�@�i���j�Y�f�|�Ɣ�Y�����`�����f�@�@�@�@�@�i���j�Y�f�|�ƒY�����`�����f
�@�@�@�@�Y�f�|�̂s�s�s�}�i�P���ϑԋȐ��j�ւ̓Y�����f�̉e��
�E�}���e���T�C�g�̏ē��ꐫ�ƊJ�n���x�ˑ���
�@�ē��ꐫ�i���E��p���ԁj�����コ���錳�f�͂b���A�l���A�l���Ȃǂŏē��ꐫ�͒Y�f���ʂŕ\���A��Ƃ���
�@�@�Y�f���ʁi�����Y�f�ʁj�����b�{�l��/6�{�r��/24�{�m��/40�{�b��/5�{�l��/4�{�u/14
�@�l���̉��x�ˑ���
�@�@�b�A�l���A�u�A�b���A�m���A�b���A�l���Ȃǂ̓}���e���T�C�g�ϑԊJ�n���x�l���������i�c���I�[�X�e�i�C�g�𑝂₷�j�A�`���A�b���Ȃǂ�
�@�グ��B
�@�@�l���_�i���j���T�T�O�|�R�T�O�~�b���|�S�O�~�l�����|�R�T�~�u���|�Q�O�~�b���� �|�P�V�~�m�����|�P�O�~�b�����|�P�O�~�l�����|�T�~�v��
�@�{�P�T�~�b�����{�R�O�~�`����
�@�@�ȂǂŎ������B���邢��
�@

�@�@�i���j�b�ʂ̉e���@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�i���j�P���b�ł̍��������̉e��
�@�@�}���e���T�C�g�ϑԂւ̓Y�������̉e��
�@�@���͗U�N�}���e���T�C�g�ϑԂ̂R�O���������艞�͂łT�O���̉��͗U�N�}���e���T�C�g���f�������鉷�x�l����
�@�@

�Ȃǂ̎�����������B
�E�������艻���f�ƃZ�����^�C�g���艻���f
�@�@�Z�����^�C�g���艻���f�E�E�E�@�b���A�u�A�l���A�l���A�m�A�v�ȂǁA�Y�������`�����₷�����f�B
�@�@�������艻���f�E�E�E�@�r���A�`���A�b���A�m���A�b���ȂǁA�t�F���C�g�i���j���Ɍŗn���錳�f�B
�E�p�[���C�g���艻���f
�@�@�r���A�b���A�l���A�b���Ȃǂ��p�[���C�g�����艻������B
�@�@��ʂɃZ�����^�C�g���艻���f�ƍ������j�Q�����f�i�a���A�`���A�r���A�o���A�s���A�r���A�r���j���p�[���C�g�����艻����B
�@�@�I�[�X�e�i�C�g���̂b���e�Ղɍ��������Ȃ��悤�ɂ��A�Z�����^�C�g�����艻���邩��ł���B
�@

�@�@�@�@�@�e���̋��͉��x�ւ̍��������̉e���Ƌ��͂b��
�E�|���ł̒Y�����`���\
�@�@�@�y�����s�����m�����u���s�����v���l�����b�����l�����e�����m���C�b���C�`���C�r��
�@�@�@�@�@�@�@�Y�����`���@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�Y�����`�����ɂ���
�@

�@�@�S�|�ʼn\�Ȏ�X�̒Y����
�@�@�S�|�ł͂U��̒Y�������`���\�ł����͂Q�̃O���[�v�ɕ�������B
�@�@��P�O���[�v�͕��G�Ȍ����\���ő�Q�O���[�v�͒P���Ȍ����\�������B
�@

�@�@�@�@�@�Y�����A�������A�퉻���̌`���G���^���s�[�i�e���R�b��j
�@�@�Y�����̍d�����ʂ͕��U���ׂ̍����Ƒ̐ϔ�Ɉˑ�����B
�@�@���ׂȕ��U���͈�ʓI�ɂu�b�A�m���b�A�s���b�A�s���b�Ȃǂ��f���\���̉��������瓾���A�l�V�b�R�A�l�U�b�A�l�Q�R�b�U�Ȃǂ̕��G�Ȍ����\����
�@��`���G���g���s�[�̉������͑e�����U���ƂȂ�B
�@�@
���e���ƂƂ��ɂu�A�`���A�s���A�b���Ȃǂ͒��������`�����A�`���A�r���A�u�A�s���Ȃǂ̂e�����_�f�ւ̐e�a�͂̑傫�����f�͎_���S��E�_���A
�`���Q�n�R�A�r���n�Q�A�s���n�Q�A�u�Q�n�T�Ȃǂ��`������B
�E�t�F���C�g�ŗn�ƒY�����ŗn
�@�@�@�r�����b�����m�����i�Y�����^�t�F���C�g�̕��z�W���P�j���v���l�����u���l�����b��
�@�@�@�@�t�F���C�g�i���j���Ɍŗn�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�Y�����l�R�b���Ɍŗn
�E�АƉ�
�@�@�e���|�m���|�b�����听���Ƃ���I�[�X�e�i�C�g�n�A�t�F���C�g�n�A�Q���n�X�e�����X�|�Ȃǂł͔M�����̉ߒ��Ŏ�X�̋����ԉ�������������
�@�Ɖ��̌����ƂȂ�B
�@�@�Б���Fe��Cr�̋����ԉ������ŁC���̒���Mo,W�CSi�CNb�CTi���̌��f���ŗn����B
�@�@�Б��̐͏o�𑣐i���錳�f�Ƃ��ẮCMo�CSi�CV�CNb�CTi�CV������C�t�ɐ͏o��}�����錳�f��Ni�CN�����C��������B
�@�@�������f�̉e����Cr���ʂŕ\���B
�@�@.Cr���ʁ�Cr�{0.31Mn�{1.76Mo�{0.97W�{2.02V�{1.58Si�{2.44Ti�{1.70Nb�{1.22Ta�|0.226Ni�|0.177Co�@
�@���̑��ԑ��ALaves���[�x�X���i�Łj�Ȃǂ��悭�`�������B
�@�@�m���𑽂��܂݂s���A�`����Y�����ꂽ�I�[�X�e�i�C�g�E�X�e�����X�|�͔M�����Ń��f���i�m���R�i�`���C�s���j�j�̐͏o�ɂ�荂�����x�����シ��B
�@

���X�e�����X�|�ɐ�����ЁA�ԁALaves�AG�AR�A�ʂȂǂ�TCP���Ń��f�i�m���R�i�`���C�s���j�j�A���h����GCP���ł���B
�@

�@�@�@�s�s�s�}�ł̊e������ԉ������ƍ��������̉e��

�@�@�e���|�b���|�m���n�R������Ԑ}
�@

�@�e���|�b���|�m���n�R������Ԑ}�̂U�T�O���ؒf��
�@

�@

�@�@�e���|�b���|�m���n�|�̐͏o��
���S�|�̊ȒP�ȕ���
�@�Y�f�|�i���ʍ|�j
�@�@�b�����������Ƃ�����̂Ő����͂b�ܗL�ʂƔM�����i�ē���A�Ă��߂��j�ɂ��B
�@����|
�@�@�d�x�A���x�A�x���A�A�ϖ��Ր��A�ϔM���A�ϐH���Ȃǂ̉��P��ړI�ɂb�ȊO�̎�X�̌��f�������������|�B
�@�@�Ă����ꐫ����A���������Y�����i�s���A�v�A�u�j�ɂ��d���ƑϔM���A�ŗn�d���i�b���A�l���A�m���A�l���A�b���A�r���A�b�j�Ȃǂ��s����B
�@�@���������ɂ͂b���i�ϐH�A�Ă����ꐫ�A�ϖ��Ձj�A�m���i�x���A�ϐH���j�A�l���A�v�A�u�i�ϔM�A�Ă����ꐫ�j�A�l���i�d���A�����A�ē��ꐫ�j�A�b���i�ϔM�j�A
�@�b���A�s���i�ϐH�A�\�ʍd�x�j�Ȃǂ�����B
�@�@
�@�@��T���ȉ����ፇ���|�A�T�|�P�O���𒆍����|�B
�@�������|
�@�@��P�O���ȏ�̍����|�ŃX�e�����X�|�ƑϔM�|����Ȃ��́B
�@�@�ϔM�|�͑ώ_���̂��߂b���@�r���A�`���A�b���|�m���A�σN���[�v�̂��߂l���A�����ň���ȒY�����l�V�b�R�`���̂��߂l���A�v�A�s���A�m���Ȃǂ��Y�������B
�@�@�T�T�O���ȏ�p�ɂ͉������ɂ������������s����B
�@�@�X�ɑϔM���̉��P�̂��߂ɂ͂m���R�i�s���C�`���j�̐͏o���ʂ����p�����B
�i�V�|�U�|�R�j�@�`�^���ւ̍��������̌���
�E�s����Q���n������Ԑ}�ƍ������f�̉e��
�@���`�^���͂W�W�Q���ȉ��ł͂g�b�o�\���i�����j�ł���ȏ�ł͂a�b�b�\���i�����j�ł��邪�A�����A�������ꂼ��̈��艻���f�Ƃ��Ă�
�@�@�������艻���f�@�@�`���A�r���A�n�A�b�A�m�ȂǁB
�@�@�������艻���f�@�@�u�A�l���A�m���A�s���ȂǁB
������B
�@
�@

�@�@�S���ŗn�^�ɂ͂y���A�g���ȂǁA��������^�ɂ͂`���A�n�A�m�A�b�ȂǁA�i���`isomorphous�j��������^�ɂ͂u�A�l���A�m���A�s���A�v�ȂǁA
�@�������͌^�ɂ͂b���A�e���A�m���A�r���A�b���A�l���Ȃǂ�����B�i�y���A�r���A�r���𒆐��I���f�Ƃ������j
�@�@���`�^���ł͂e���A�b�A�n�A�m�A�g�Ȃǂ��s�����ŋ��x�͎_�f���ʂŕ]�������B�_�f���ʂ�
�@�@�@�_�f���ʁ��n���{�Q�D�O�m���{�O�D�U�V�b��
�@�Ȃǂ���Ă���Ă���B
�@�@�����艻���f�ɂ�
�@�@�@�`�����ʁ��`����+�O�D�P�V�y�����{�O�D�R�R�r�����{�P�O�n���{�P�U�D�S�m���{�P�P�D�V�b��
�@�Ȃǂ���Ă���Ă���B
�@�@�����艻���f�ɂ�
�@�@�@�l�����ʁ��l�����{�O�D�Q�s�����{�O�D�Q�W�m�����{�O�D�S�v���{0.67V���{�P�D�Q�T�b�����{�P�D�Q�T�m�����{�P�D�V�l�����{�P�D�V�b�����{�Q�D�T�e����
�@�@�@�u���ʁ��u���{�P�D�T�l�����{�Q�D�S�b�����{�R�D�W�e�����{�P�D�V�m�����{�O�D�U�v���{�O�D�S�m����
�@�@�������͌^�ɂ�
�@�@�@�e�����ʁ��e�����{�O�D�V�b�����{�O�D�V�l�����{�O�D�T�b�����{�O�D�T�m����
�@�Ȃǂ���Ă���Ă���B
�E��Ȃs���Q���n��Ԑ}

�@�@�@�s���|�y���n��Ԑ}
�@�@

�@�@�@�s���|�`���n��Ԑ}
�@�@
�@

�@�@�@�@�s���|�u�n��Ԑ}
�@

�@�@�@�@�@�@�@�s���|�b���n��Ԑ}
�@�@�@

�@�@�@�@�@�@�@�r���|�s���n��Ԑ}
�E�}���e���T�C�g���ƃ֑�
�@�@�������烿���ւ̕ϑԂ͊j�����ƃ}���e���T�C�g�^�i����f�^�j�ŋN����B
�@�@���`�^���ƒ�`�^�������͋}��łQ��ނ̓����}���e���T�C�g���f�i�Z�����j�A���h�i�Ε����j����B
�@�@�ʏ�̓��f�������A���h�͎�ɂl���A�m���A�s�����邢�͂`���Ƃu���܂ރ`�^�������i�����艻���f����r�I�����j�Ő�����B
�@�@�}���e���T�C�g�ϑԊJ�n���x�������t�߂ɂ���j�Anear���^�����ł͉��͗U�N�}���e���T�C�g����������B
�@�@�s���̃}���e���T�C�g�͍d���Ȃ��A�ނ���_�炩���B
�@
�@���[���`�^���ƃ��`�^���ł͏Ă�����Ǝ����ŏ�������̂���̕ϑԂɂ��ւƃ��f�̂Q�̏����葊��������B
�@�ւ͉t�I�Ŗ��g�U�̕ψʌ^�ϑԂ����}���e���T�C�g�ƈقȂ�\�ʋN���͐����Ȃ��B�@
�@�T�T�O���ł̎����Ő�����M�I�i�����jisothermal�ւƏĂ�����Ő������M�I�i�}��jathermal�ւ�����B
�@���f�͂Q�O�O�|�T�O�O���Ő�����}�g���b�N�X�ɐ����Ȃa�b�b�]�[���ł���B

�@�@�@�s�������̂l���̑g���ˑ�
�@

�@�@�@

�@�@�@�@���`isomorphous�`�^�������̏�Ԑ}
�E�`�^�������̎��
�@���`�^���s���͂W�W�Q����荂���ł͂������̃����A�ቷ�ł͂������̃��������������ł̓��^�A�inear���^�A�j���{���^�A�inear���^�A�j���^������B
�@�@���^
�@�@�@�@���̈悩��̏Ă�����Ń��f�Ǝc������������B
�@�@�@�@�T�|�U���`�����Q�i�s���R�`���A�K�����j����B
�@�@�@�@���ƓI���`�^���@�@���_�f����
�@�@�@�@�s���|�T�`���|�Q�D�T�r��
�@�@

�@�@�����艻�`�^���̏�Ԑ}
�@�@�j�Anear���^
�@�@�@�@���ʁi�P�O���ȉ��j�̃��������݂��鍇���B
�@�@�@�@���{���̈�A���̈悩��Ă�����Ń��̓}���e���T�C�g�ϑԁ@���f����B�����Ŕ��ׂȃ��͏o�B
�@�@�@�@�s���|�W�`���|�P�l���|�P�u�@�@
�@�@�@�@�s���|�U�`���|�Q�r���|�S�y���|�Q�l���@�@
�@�@���{���^
�@�@�@�@���{���̈�A���̈悩��Ă�����Ń��c���B
�@�@�@�@������Ă�����ł͂l���ȉ��Ń}���e���T�C�g�ϑԂŃ��f�ƃ��h��������B
�@�@�@�@�}���e���T�C�g�̏Ă��߂��Ń��ƃ����邢�̓��Ɖ�����
�@�@�@�@�c�����͎����ŃւƂȂ�B
�@�@�@�@�s���|�U�`���|�S�u
�@�@�@�@�s���|�U�`���|�U�u�|�Q�r��
�@�@�j�Anear���^
�@�@�@�@�Ă�����ł̓}���e���T�C�g�ϑԂ͂����炸�֑�����B
�@�@�@�@���͗U�N�}���e���T�C�g�ϑԂ��N�����B
�@�@�@�@�s���|�P�O�u�|�Q�e���|�R�`��
�@�@���^
�@�@�@�@�l�����ʂ��Q�T�ȉ��ŏ�������^�A�U�ȉ��Ńj�A���^�B�@�@�@�@
�@�@�@��������^
�@�@�@�@�@�@�l���������ȉ��i���̈悩��̗�p�Ń}���e���T�C�g�ϑԂ��N�����Ȃ��j�ŁA�}��Ń����ƂȂ�A�P�������Ń��{���g�D
�@�@�@�@�@�ɂ��邱�Ƃ��ł���B
�@�@�@�@�@�@�s���|�W�l���|�W�u�|�Q�e���|�R�`���@�@
�@�@�@�@�@�@�s���|�R�`���|�W�u�|�U�b���|�S�y���|�S�l���@
�@�@�@�@�@�@�s���|�P�T�u�|�R�b���|�R�`���|�R�r���@�@�@�@
�@�@�@�@�@�@�s���|�P�R�u�|�P�P�b���|�R�`���@
�@�@�@�@�@�@�s���|�P�P�D�T�l���|�U�y���|�S�D�T�r���@
�@�@�@������^
�@�@�@�@�@�@�P�������Ń��{���g�D�ɂ��邱�Ƃ��ł��Ȃ��B
�@�@�@�@�@�@�s���|�R�T�u�|�P�T�b��
�@�@�@�@�@�@�s���|�R�O�l��

�i�V�|�U�|�S�j�@�j�b�P������ƃR�o���g����@
�i���j�j�b�P�������
�@�ϔM�|�����鍂�����x����ёϐH���̗D�ꂽ������ϔM�������邢�͒��ϔM�����Ȃ����������isuper alloy�j�ƌĂсA�q��@�p
�i�W�F�b�g�E�G���W���E�^�[�r���j�A���d�p�i�K�X�E�^�[�r���j�ȂǂɎg�p����邪���̒��S�̓j�b�P������ł���B
�@Special Metals Corporation�̃C���R�l��Inconel�A�C���R���CIncoloy�A�j���j�b�NNimonic�A���[�f�B���b�gUdimet
�@United Technologies,Inc�̃��X�p���CWaspaloy
�@Haynes International,Inc.�̃n�C�l�XHaynes�A�n�X�e���CHastelloy
�@Carpenter�Ђ̃J�[�y���^�[Carpenter
�@General Electric�̃��lRene
�Ȃǂ��m���Ă���B
�@�m���͂e�b�b�\���������Z�_�P�S�T�T���ł���B���̑��͂e���|�m���n��Ԑ}�����ƂɃ����i�I�[�X�e�i�C�g�j�ƌĂ��B
�@�j�b�P��������́A�ŗn�����^�����ƁA�m��3�i�`���A�s���j����Ȃ���f�����܂ސ͏o�����^�����Ƃɑ�ʂ���A����ɁA���f���̑������͏o�^�����́A
�M�ԉ��H�������A��ʂɒ����@�╲������@�ɂ�萻������A���f�����ɏ��Ȃ���͏o�^�����́A�b���A�������̔M�ԉ��H�ɂ���Đ��������B
�@
�@�j�b�P��������̓Y��������
�@�@�@���`�����f�@�b���A�b���A�l���A�v�A�e���A�q���ȂǂŌŗn�����������B
�@�@�@���f�`�����f�@�`���A�s���A�s���ȂǂŋK���\���k�P�Q�i�������j�̂m���R�i�`���A�s���j�̐͏o�d���������B
�@�@�@�@�@�@���f���̂m���R�i�`���A�s���j�͕ꑊ���ɐ����I�ł����x�㏸�ɔ������x���㏸����Ƃ������������B
�@�@�@�@�@�@�m���R�m���͐������łc�O���K���\�����������h�i�K���}�E�_�u���E�v���C���j���ƌĂ��B
�@�@�@�Y�����`�����f�@�@�b���A�l���A�v�A�m���A�s���A�s���ȂǂŒY�������`�����͏o�d���Ɋ�^����B
�@�@�@�@�@�@�l�b�^�@�m���b�A�s���b�A�s���b�A�g���b�ȂǁA�����ň���B
�@�@�@�@�@�@�l�U�b�^�@�i�m���C�b���C�l���j�U�b
�@�@�@�@�@�@�l�Q�R�b�U�^�@�b���Q�R�b�U
�@�@�@���E�ΐ͌��f�@�a�A�y���ȂǁB���E�����t�H���W�[�����P���A�σN���[�v��������B
�@�@�@���̑��퉻���l�R�a�Q�A�]�����ȂǁB
�@�@
�@�@�@�������ɐ����鏀����ȋ����ԉ������ɂ͂s�b�o���Ƃf�b�o��������B
�@�@�@�s�b�o��
�@�@�@�@�Ώ̓x���Ⴍ�A�ꑊ�ɔ��ŐƉ��̌����ƂȂ�₷���B
�@�@�@�@Laves���`�Q�a�@�i�m���C�b���C�e���j�Q�i�l���C�s���C�m���j
�@�@�@�@�Ё@�b���b��
�@�@�@�@�ʁ@�i�e���C�b���j�V�i�l���C�v�j�U
�@�@�@�@�ԁA�f�A�q�E�E�E
�@�@�@�f�b�o��
�@�@�@�@�ꑊ�ɐ����I�Ő͏o�d�����ʂ��������Ƃ������B
�@�@�@�@���f�A���h
�@�@�@�@���@�m���R�m���A�Ε����A���h���̒����Ԏ����Ő�����B
�@�@�@�@�ő��@�m���R�s��
�@�@

�@�@�@�@�@�m���̃����ւ̓Y�������̗n���
�@
�@

�@�@�@�@�@���ALaves���̂s�s�s�}�ihttp://www.jnes.go.jp/content/000117527.pdf�@�i�m�d�r�����j
�@

�@�@�@�@���h�̂s�s�s�}�ihttp://www.jnes.go.jp/content/000117527.pdf�@�i�m�d�r�����j
�@�@

�@�@�@�ihttp://www.jnes.go.jp/content/000117527.pdf�@�i�m�d�r�����j
�i���j�R�o���g�����
�@�b���͂S�P�V���ł��������炆�����ւ̓��f�ϑԂ��s���B
�@�b���ɂ͂m��������̃��f���̂悤�ȍ������x����������炷�ǍD�Ȑ͏o�������݂��Ȃ����ߑϔM�����Ƃ��Ă͂��܂�g�p����Ȃ��B
�@�b��������͎�ɂl�Q�R�b�U��l�b�^�Y�������ɂ��͏o��������Ă���B
�@�k�P�Q�^�\����L����b���R�s���C�b���R�s�����͗Z�_���Ⴍ�������荂���ł̈��萫�ɖR�����������x����̌��ʂ����܂�����炳�Ȃ��B
�@

�@�R�o���g����͒Y�����A�]�����̐͏o�𗘗p�����ϖ��Ս����Ƃ��Ď�ɗ��p����Ă���B
�@�o�C�^���E��Vitallium�@�b���|�b���|�l���n
�@Co-30Cr-5�`6Mo-�`1Si-�`1Mn�A���ȗp�A�l�H�߂Ȃǐ��̍ޗ��Ƃ��ė��p�B
�@�X�e���C�gStellite�@�b���|�b���|�v�n
�@Co-25�`30Cr-2�`15W-�`3Ni�`3Fe-0.25�`3.3C-�`2Si�A��Ɂi�b���C�v�j23�b6�܂��́i�b���C�v�j7�b3�̐͏o�d���𗘗p�B
�@�g���o���CTribaloy�@�b���|�l���|�b���n
�@Co-28Mo-9Cr-2.5Si�AMo2Co3Si�̐͏o�d���𗘗p�B
�@�R�o���g��ϔM������Co-20-�`23Cr-7�`15W-10�`22Ni-�`3Fe-0.1�`0.6C����\�I�g���ł���B
�i�V�|�U�|�T�j�W���R�j�A�ւ̓Y�������̌���
�@�@
�@�W���R�j�A�i�y���n�Q�_���W���R�j�E���j�ɂ͒ቷ����P�Ώ��l�i���x�T�D�T�U�j�A�������s�i���x�U�D�P�j�A����cubic���b������A�����t�߂ł�
�P�Ώ��ł��邪�P�Q�O�O���t�߂̍������̐���������ቷ���̒P�Ώ��ւ̑��ϑԂŖ�S���̑̐ϑ������j����N�����B
�@���̂��߈��艻�܂Ə̂���l���n�A�b���n�y�тx�Q�n�R�A�g���Q�n�R�A�b���n�Q���̊�y�ގ_�����̓Y���i�y���C�I�����傫�ȃC�I�����a�����C�I���j��
�������̗���cubic�����邢�͐������������܂ň��艻�����邱�Ƃ��s�Ȃ��A��������艻�W���R�j�A�Ƃ����B
�@�����������艻�������ꍇ�ɂ͗��������艻�W���R�j�A�i�L���[�r�b�N�E�W���R�j�A�j�Ƃ����A���������艻�W���R�j�A��菭�Ȃ��ʂ̈��艻��
�y�ї��a�������Ő����������艻���������̂͐������W���R�j�A�Ƃ����B
�@�P�Ɉ��艻�W���R�j�A�Ƃ����ꍇ�ʏ�͗��������艻�W���R�j�A���w���B
�@�P�Ώ��A�������A���������Q���ȏ㍬�݂�����̂����艻�W���R�j�A�Ƃ����B
�@�i�P�Ώ��Ɛ��������邢�͒P�Ώ��Ɨ��������邢�͐������Ɨ������̂Q�����݁A���邢�͒P�Ώ��A�������A�������̂R�����݁j
�@�������͉��͂ŒP�Ώ��ɕω����鉞�͗U�N�ϑԁi�}���e���T�C�g�^�ϑԁj���N�����B
�@

�@

�@�@�@�@�@�y���n�Q�|�x�Q�n�R��Ԑ}
�i�W�j�@�g�U�̖��
�@�EKirkendall����
�@�@�@���݊g�U�ɂ�����g�U�W���̈Ⴂ��Kirkendall���ʂ��䂫�N�����B
�@�@�@���Ƃ��`�̂a�ɑ���g�U�W�����a�̂`�ɑ���g�U�W�����傫���Ƃ`���̊g�U�ɂ�錴�q�ړ��ɂ݂����a����
�@�@�g�U�ɂ�錴�q�⋋���s���Ȃ����߂`���Ƀ{�C�h���������邱�ƂɂȂ�B
�@�@�@�`���߂����Ƃr���n�����͂Ŗ��ƂȂ邱�Ƃ�����B
�@�E����g�U�iuphill diffusion�A�t�g�U�j
�@�@�@�g�U�̋쓮�͂��g�U���f�̔Z�x���z�ȊO�i�����g���A���́A���x�j�ł���ꍇ�ɐ�����g�U���f�̔Z�x���z�ɋt�炤�g�U�B
�@�@�@Darken���Y�f�|�̗n�ڂ�Si���܂܂Ȃ���Y�f�̍|����Si���܂ލ��Y�f�̍|�֒Y�f���g�U���邱�Ƃŏؖ������B
�@�@�@�Q���n�ł̓X�s�m�[�_�������Ő�����B
�@���G���N�g���E�}�C�O���[�V����
�@�@�@�h�b�i�W�ω�H�j�̂`���z���ɑ�d���𗬂����Ƃ��̒f���̌����̓G���N�g���E�}�C�O���[�V�����Ƃ��Đ�������Ă���B
�@�@�@����͔z���ɓd���������Ɠd���i�d�q���j�͋������q�ɓd�q���͂�^����A�܂�d�q�̏Փ˂ɂ���ċ������q���J�\�[�h
�@�@������A�m�[�h���Ɉړ����A�J�\�[�h���Ƀ{�C�h���`������f�����A�A�m�[�h���Ƀq���b�N�i�ˋN�j��E�C�X�J���`�������
�@�@�Ƃ������̂ł���B
�@�@�@�Ȃ��z���ɖc�������Ȃǂň������艞�͂������邱�Ƃɂ��������q���ړ����{�C�h���`������f�����錻�ۂ�
�@�@�X�g���X�E�}�C�O���[�V�����Ƃ����B
�@���o���A�E���^���ƃA���_�[�E�o���v�E���^���t�a�l�i�o���v���n�����j���邢�̓A���_�[�E�o���A�E���^���t�a�l
�@�@�@�W�ω�H���ŋ����̊g�U�A�����h�~�̂��߂Ɍ`�����������w���o���A�E���^���A��A���w�Ƃ̖�������M�c�����̓K�����d�v�B
�@�@�@���ɔz���i�d�Ɂj�ƃo���v�i���ɂ͂j�Ƃ̊ԂɌ`���������̂��t�a�l�i�A���_�[�E�o���v�E���^�����邢�̓A���_�[�E�o���A�E���^���j
�@�@�@�����W�ω�H�Őڍ��̐R���^�N�g���ł́AAl�z���d�ɂ�Si���v���Z�X���ɍ����Ŕ������ăX�p�C�N���`�����A�ڍ��ʂ܂�Al��
�@�@�˂������A�ڍ����j���̂�����邽�߁AAl�̑����Al-Si�������g�p������Al�z���̉��Ƀo���A���^�����`�������肵�Ă����B
�@�@�@�܂��z�������Ɛ≏���̔M�c�������ɂ��X�g���X�E�}�C�O���[�V�������������A���̑�Ƃ��Ă��o���A�E���^�����`������悤�ɂȂ����B
�@�@�@���̂悤�ɂ���Si�܂��͐≏���Ɣz���iAl�ACu�j�̊ԁA���Ƀ_�}�V���Ƃ���Cu�z���̊ԂɃo���A�E���^�����`�������B
�@�@�@�`���ł͂s���m�A�b���ł͂s���A�s���m�Ȃǂ��p������B
�@�@�@�܂��͂o���v���ɂo���t���[�͂o���v�͔������������i�H���j�����͊ɘa���ɂ��������ߓK���ȃo���A�E���^�����`����
�@�@�K�v�Ƃ����B
�i�X�j�@���H�E�����g�D
�i�X�|�P�j�@�W���g�D
�@�����͑������̂Œʏ�͌X�̌������͖������ɔz�����Ă��邪�A���̑������̂�
�@����̕����i�D����ʁj�ɔz������ꍇ�����肱����W���g�Dtexture�Ƃ����B�@
�@�E���H�W���g�D
�@�@������Y�����H�i�����A�����������̗�ԉ��H�j�����ꍇ�ɐ�����W���g�D�B
�@�E�����W���g�D
�@�@�������H���s�������Ƃ̔M�����i�Ă��Ȃ܂��j�ɂ��W���g�D�B
�i�X�|�Q�j�@����
�@�����H���ꂽ���������M����ƁA���q�̍Ĕz������Ђ��݂̂Ȃ������ɖ߂�A������Č����Ƃ����B
�@���ۂ͍Č����̑O�ɂ܂��_���ׂ̏��ł�]�ʂ̍Ĕz�N���肱����Ƃ����B
�@�X�ɉ��M���s���ƐV�����������̐����Ɛ����ɂ��]�ʂ̏��Ȃ��V�����g�D�ƂȂ��╨���I������
�傫�ȕω����N����B
�@���̉ߒ����P���Č����i�ÓI�Č����j�Ƃ����B
�@���I�Č����͍����ł̉��H���i���͉��j�ɋN����Č����B
�@
�@�������͉��x�⏞�c���x���q�iZener-Hollomon���q�j�y��(d��/dt)exp�i�p�^�q�s�j�Ɏx�z����A
�y���傫���قǁA�c���x���傫���قǁA���x���Ⴂ�قǍČ������͏������Ȃ�B
�@�X�ɍ������邢�͒����Ԃ̉��M���s���Ɠ���̌����������̌�������H���Č������̋}�����A�e�剻��
�N����ꍇ�����肱����Q���Č����i�ُ팋���������j�Ƃ����B
���]�f�|�ł͂Q���Č����Ő������W���g�D�̔z�����ʂ��ς��R���Č������N����B
�@�@�R���Č����͂Q���Č����Ŏc�������������������Q���Č����Ő������傫�Ȍ�������H���Đ������邱��
�@�ɂ��N����B
�����헱�����ł͌ÓT�I�ڋߕ��@�Ƃ���
�@�@�@����������
��Burke��Turnbull�͂����O�D�T�Ƃ����B�]���Ĉ�ʓI�ɂ�
�@�@���Q�����O�Q�{���������O�Q�{���f���Eexp�i�|Q/RT�j
�@�ُ헱�����ł́A��Q����Zener�̃s�j���O��������Q���̗��a���ƃ}�g���b�N�X���aR0��
�@�@�@R0=�S���^�R���@�@�@�@���F���U���q�̑̐ϔ䗦
�ɂ���Q�����������A�̐ϔ䗦���傫����Η��a���������Ȃ�B
�@Gladman�̓}�g���b�N�XR0�̗�������j�~�����Q���̗ՊE�a���̊W�Ƃ���
�@�@�@
 �@�@Z�F�������a��R0�̔�
�@�@Z�F�������a��R0�̔������B�ُ헱�����͑�Q���̌a���㎮�̂������Ƃ��ɔ������A�ՊE�a�����������قNjN����₷�����ƂɂȂ�B
�@�܂��}�g���b�N�X���a���������قǂ�����₷���B
���irecovery�j�A�Č����A�����������̈�A�̉ߒ����irestoration�j�Ə̂��邱�Ƃ�����B
�E�z�����K�X(homologous)���x�i�������x�j
�@�@��Ή��x�i�j�j�\���ŁA�Z�_�ŋK�i�����ꂽ���x�B�܂�s�^�s���B
�@�@���x�������A�Ⴂ�Ə̂���ꍇ���̔F���͂��̍ޗ��̗Z�_�ɂ���ĈقȂ邪�A�z�����K�X���x�ŕ\������ƗZ�_���̉e�������ē���I����
�@�i���꒼���A�Ȑ���ɂ̂�Ȃǁj�ł���ꍇ�������B
�@�@���Ƃ��Č������x�s�������͂s�������^�s�����O�D�S�`�O�D�U�ŁA�܂�Č������x�O�D�S�s������O�D�U�s���Ŗڈ��͂s���^�Q�Ƃ����B
�@�@�N���[�v�i�艷�A�艞�͂ł̎��Ԃɂ��ό`���ہj���ۂł��悭���p����A�N���[�v�͂�͂�O�D�T�s���ȏ�Ō����ɂȂ�B
�i�X�|�R�j�@�A���Č����i���̏�Č����j�ƕs�A���Č���
�@�ʏ�̗�ԉ��H�ł͉��H�ɂ���Đ����������������Ԃ̕��ʍ��i�X�p�j���������i���X�p�F�P�T�x�ȉ��j�A���̏��X�p�ł�
�ÓI�Č����ɂ�舟����������j�����Ɛ����ɂ��Č����������s�A���Č����Ƃ����B�s�A���Č����ł͍Č������͈�������
�̏��Ȃ��Ƃ����{�̑傫���ƂȂ�B�i���H�x���̏ꍇ�̐ÓI�Č����ɂ��s�A���Č����j
�@����ɑ��ቷ�ŋ����H���{���A�����������X�p�i�P�T�x�ȏ�j�Ƃ���ƁA���Ȃ킿������]�ɂ�舟�������̕��ʍ����A���I�ɑ�����
��X�p������ƈ��������͂��̏�Ō������ƂȂ肱����i���I�j�A���Č����Ƃ����B�i���H�x��̏ꍇ�̓��I�Č����ɂ��A���Č����j
�@�s�A���Č����ł͂P�ʂ��ȉ��̔����͕s�\�ł��邪�A���Č����ɂ��P�ʂ��ȉ��̔������\�ł���B
�@����`�������Ȃǂł͍����A��c�ݑ��x�Ō����������������E���x�̌��݂ɝG���ɂȂ�A�X�ɗ��E�����������ɂȂ蕔���I�ɗ��E��
�ڐG����悤�ɂȂ��čŏI�I�ɂ�����A�����ȓ����������ƂȂ��w�I���I�Č���������B
�@���Ȃ킿�Č�����
�@�@�ÓI�Č����@�E�E�E�s�A���Č���
�@�@���I����
�@�@�@�@�s�A������
�@�@�@�@�A������
�@�@�@�@�w�I����
�ƕ��ނ����B
�i�X�|�S�j�@���q�U�N�j�����oarticle �rtimulated �mucleation
�@�����ɑ�Q�����q�i�͏o�Ȃ������U���j������ꍇ�A��Q�����q�͏����ɂ��Č����x�����ʂƍČ������i���ʂ̂����ꂩ�������B
�@��ʂɍd���đ傫���i���P�ʂ��j�ꍇ�ł͗��q�U�N�j�����o�r�m���N����ꍇ������B
�@�܂����̋��E�͑�Q�����q�̗��q�̐ϗ��e���Ɨ��q�a�����@�e���^�����O�D�Q�ʂ��ɂ���A�@�e���^�����O�D�Q�ʂ��ōČ����x�����ʁi�[�[�i�[�E
�s�j���O�j�����������Ƃ���A���������Č����������̂��߂ɂ͕��U���q�̑̐ς𑽂����邩���ׂɂ���K�v������B
�i�X�|�T�j�@�g�U�U�N����
�@�Z�_�̂P�^�R���x�̉��x�̗��E�g�U�ɔ�ב̐ϊg�U�������ł�����x�̉��x�ŁA�������̗��E�ɉ����Ă̗n�����f�i�g���̕s�ψ�
�ɂ��j�̊g�U�ɂ��A���E���ړ����A���ɍ����w�i�g���̕s�A���ɈقȂ�̈�j�������邱�Ƃ�����A������g�U�U�N���E�c�h�f�l�Ƃ����A
�X�ɍČ����ɂ�荇�����i�������ꑊ�Ƒg�����s�A���ɈقȂ�Č����̈�j��������ꍇ���g�U�U�N�Č����c�h�q�Ƃ����B�e���i�y���j�A�b���i�y���j
�b���i�`���j�A�`���i�`���j�A�`���i�o���j�A�v�i�b���j�ȂǂŌ�����B
�i�X�|�U�j�@�����̒P�����E�C�X�Jwhisker�i�Ђ������j
�@�d�C�߂��������r���A�y���i�����|���j�A�b���Ȃǂ���P�����̃E�C�X�J���������鎖���悭�m���Ă���B
�@�T�^�I�ɂ͑����P�`�Q�ʂ��A�����O�D�P�`�P�O�����ő����͐j���m�W���[���i���߁j��A�q���C�b�N�i���u�j��Ȃǂ�������B
�@�j��̂��̂͐^�������Ȃ��̂̂ق��ɋȂ������肷����̂�����B
�@�����E�C�X�J�͂߂�����̐������Ԃ������A�퉷�ł������A��������B
�@�r���̃E�C�X�J�͂o���Ƃ̍������ʼn��P���ꂽ���o���t���[���̓����ōĔR�����B
�@�r���̂o���t���[�������ł͂a������Ԍ��ʂ�����Ƃ���邪�Ƃ��Ȃ铙�̌��_������B
�@�����@�\�ł͂������̓]�ʃ��f������Ă��ꂽ���^�₪������Ă���B
�@�܂��Č����Ƃ����������B
�@������ɂ��戳�k���͂��쓮�͂Ƃ��邱�Ƃ��F�߂��Ă���B
�@�����͂u�k�r�@�\�ƈقȂ�E�C�X�J�̍������琬������B
�@�r���ɂ��Ă͏ڂ����������ꈳ�k���͂̌����Ƃ��āA�߂����̐͏o�̍ۂ̎c�����͂̑���
�@�@�����ł͂b�����n�ɑ������ԉ������b���U�r���T�̐����ɂ��B�m���w���`�����邱�Ƃ�P�T�O���t�߂̔M���������ʂ�����B
�@�@���x�T�C�N���ɂ����́A���n�Ƃ̔M�c�����ɂ��A���Ȃ����`��ƂȂ�₷���B�����������P�O�ʂ��Ƒ傫���Ȃ�Ȃ��B
�@�@�_���E���H�ɂ�蔭�����鉞�͂ɂ��B
�@�@�O���ɂ����́A�R�l�N�^�[�ȂǂŔ����B
����ʂ���Ă���B
�@�܂��r���E�C�X�J�ɂ͂߂�����������Ԃ��o�Ă�����萬������P�����i���r���j�̐^���E�C�X�J�̂ق��ɁA���d���r���߂������ɔ������A
�߂�����͐������Ȃ��������i���r���ƃ��r���j�̋[���E�C�X�J������Ƃ����B
�@�E�C�X�J�͂`���A�`���A�`���Ȃǂł̔���������Ă���B
�@�܂��r���`���b���͂�r���o���͂���̃E�C�X�J����������Ă���B
,�@�`������r���͋C�ł`���Q�r�E�C�X�J����������B���̂`���Q�r�E�C�X�J���}��`��i��̂ɕ��ʓI�ł͂Ȃ����̓I�A��̂ɕ��ʓI�Ȃ��̂̓f���h���C�g�j
�̃E�C�X�J����������B
�@�E�C�X�J�͐��������n���狟�������^���E�C�X�J�Ƃ`���Q�r�̂悤�Ȕ����ɂ���^���E�C�X�J�ɋ�ʂ��邱�Ƃ�����B
���C������̒P�����E�C�X�J����
�@�C�������i�u�r�����j�ɂ���Ă��悭�E�C�X�J����������B�����@�\�Ƃ��čŏ��ɍl����ꂽ�̂͂点��]�ʐ������^�⎋����Ă���B
�@�i���Ȃ��Ƃ����ׂĂ̂u�r�E�C�X�J�͐����ł��Ȃ��j
�@�����@�\�������炩�ɂȂ��Ă���̂͂u�k�r�ivapor-liquid-solid�j�@�\�ƌĂ����̂łr�����L���ł���B
�@�u�k�r�@�\�ł͋C�����t�����o�R���ăE�C�X�J����������B
�@�������}�ŁA��̏�ɐG�}�ƂȂ镨�������݂��i���j�A���M�ŗn�Z���i���j�A��̂�n�������t�H���`�����i���j�A���̉t�H���C������
�E�C�X�J�������z�����A�O�a���t�H�����ɃE�C�X�J���͏o���i���j�A�E�C�X�J��[�ɉt�H���������ԂŃE�C�X�J����[���琬�����Ă����i���j
�Ƃ������̂ŁA�r����̂`���ɂ��r���`���̋����`���ɂ��t�H�`���ƋC������̂r�������ɂ��r���E�C�X�J������A�O���t�@�C�g��̂e���Ƃe���n�Z
�ɂ��b��n�������t�H�̌`���ƋC������̂b�A�r�������ɂ��r���b�E�C�X�J�����Ȃǂ��������L���ł���

�@�@�u�k�r�@�\�ɂ��E�C�X�J�����͎��}
�i�P�O�j�@�������E
�i�P�O�|�P�j�@���ꗱ�E�ƌX�p���E
�E���ꗱ�E
�@�@�E�ʂ���]���ɐ����ȗ��E�A�点��]�ʂ̏W���Ō`���B
�E�X�p���E
�@�@�E�ʂ���]���ɕ��s�ȗ��E�A�n��]�ʂ̏W���Ō`���B
�i�P�O�|�Q�j�@�Ή��i�q�_�Ƈ��l
�E�Ή��i�q�_CLS Coincidence Lattice Site
�@�@���ꌋ���\���̂Q�����������]���̎��͂ɃƉ�]�������Ƃ��ɐ�����Q�̌����̎����I�ɏd�Ȃ�i�q�_�B
�@�@�}�͒P���i�q�����O�O�P�����ɂR�U�D�T�Q�x��]�����ꍇ�őΉ��i�q�_�����Ŏ����A
�@�@

�E���l
�@�@���Ƃ̌����i�q�̒P�ʖE�̐ςƑΉ��i�q�̒P�ʖE�̐ς̔�A���邢�͑Ή��i�q�_�̖��x�̋t���B
�@�@�����������قǎ��������Z���A�K���x�������B���͊�l���Ƃ�B
�@
�i�P�O�|�R�j�@���X�p���E
�@���X�p���E�͂Q�̗��E�̌������̂Ȃ��p�x�A���ʊp�̍��i�X�p�A�~�X�I���G���e�[�V�����j���P�T�x�����̂��̂ň����E�B
�@���X�p���E�͇��P��Read-shockley���f���i�n��]�ʂ̏W���AE����E�O�ƁiA-ln�Ɓj�j�Ő��������B
�i�P�O�|�S�j�@�Ή����E
�@����̉�]�p�ɂ��Č`�����������I���q�z��܂�Ή��i�q�_�������E�B
�@���ʊW�̂��ꂪ�P�T���^���P�^�Q�ȉ��Ȃ�Ή����E�̗��_���K�p�ł���B�iBrandon�̏����j
�@�E��X�p���E�i�Ή����E�j�@
�@�@�@�X�p���P�T�x���X�p���E
�@�@�@���R�͑o���A���Rn�͑o���ɕt�����Č����闱�E
�@�@�@���@�`�i�Q�X�j
�@���Ή����E�̈Ӌ`
�@�@�@�Ή����E�͗��E�G�l���M�[���Ⴍ����Ƃ���A���ۂɑ����̕����̑������őΉ����E���悭�ώ@�����B
�@�@

�i�P�O�|�T�j�@�����_�����E�i��ʗ��E�j���q
�@���̑傫�����́A���Ƃ��Q�X������̂������_�����E�Ƃ���ꍇ�������B
�@
���قȂ錋���\���̗��E�̊E�ʂł���ّ��E�ʂɂ�Bollmann�̂n�|�i�q���_�����p�����B
�@�n�|�i�q���_�ł͊i�q�_�̑���Ƀp�^�[���i�Ή������_�j�̏d�Ȃ���l����B
�i�P�O�|�U�j�@�\�����j�b�g
�@�@���E�͌����ƈقȂ錴�q�N���X�^�[�ł���\�����j�b�g�̑g�ݍ��킹�ƍl������B
�i�P�O�|�V�j�@���E���i
�@���E�͂Q�̌����̋��ʉ�]���A��]�p�A���E�ʕ��ʂȂǂ����q�Ƃ��闱�E���i�ɂ���Ă��̓������e������B
�i�P�O�|�X�j�@���E�ΐ�
�@�ΐ͂Ƃ����p��͋����w�ł͒ʏ�A�Ìʼnߒ��ɊW���Ďg�p�����B
�@�n�Z�����̋Ìł̉ߒ��Œ���ɂ͓���I�K�͂̔Z�x���������A����̓}�N���ΐ͂ƌĂ��B
�@�܂��A�f���h���C�g�ƃf���h���C�g�Ԃ̋�Ԃ̊Ԃɂ̓ʂ��K�͂̔Z�x���������A����̓~�N���ΐ͂ƌĂ��B
�@�����ΐ͂͗Z�_�ł̌ő����Ɖt�����̉��w�g���̍��ɂ�萶����B
�@�ÌŁE�������ɂ�����ΐ͂ɑ��A���E�ł̋Ǖ��I���w�����̕ω��ŗ��E�j��◱�E�̐Ɖ��A���E���H�̌����ƂȂ�ΐ́\���E�ΐ͂�����B
�@���E�ΐ͂͂����K�͂Ɍ����邪�Z�x���̓}�N������у~�N���ΐ͂�肩�Ȃ�傫���B
�@�����ł̗n�����f�̗��E�ΐ͕͂��t�ΐ͂Ɣt�ΐ͂ɕ�������B
�@���t�ΐ͔͂M�͊w�I�ߒ��ō����n�̕��t���Ő�����B
�@���̕ΐ̗͂ʂ̓A�j�[�����x�̒ቺ����у}�g���N�X���̗n�����f�Z�x�̑����ƂƂ��ɑ�������B
�@���t�ΐ͂ɂ̓}�N���[���̓��v�M�͊w�I�L�q���L���ł���B
�@���t�ΐ͂͊i�q�ʒu�̗n���̃G�l���M�[�ƁA���E�̗n���̃G�l���M�[�̍��ɋN�����A�s�������f�����������ɑ��݂���ꍇ�̃G�l���M�[�́C
���ꂪ�������E�ɑ��݂���ꍇ���傫���B���̃G�l���M�[�̍����ΐ͂̋쓮�͂ƂȂ�B�}�N���[���͂����e���c�݃G�l���M�[�ɂ���Č��ς������B
�@���t�ΐ͗ʂ͒ቷ�قǑ傫���C���x�㏸�ɔ����Č�������B����C�ቷ�ł͌��q�g�U���x�����������߁C�s�����͗��E�֗e�Ղɂ͈ړ��ł��Ȃ����A
���x�㏸�ɔ����Ċg�U���x�����傷��ƁC�ΐ͂��\�ɂȂ�B���ǁA���t�ΐ͗ʂƕ��t��Ԃ߂Â��g�U���x�Ƃ̒ނ荇���ł��܂�B
�@����ɑ��t�ΐ͂ł͉��x�㏸�ƂƂ��ɕΐ͂̓x�������㏸���邪�A�������Ȃ��Ă������͋ώ������邱�Ƃ��\�ł���B
�@���t�ΐ͗ʂ͒P���q�w�Ȃ��������q�w�ł��邪�i�䂦�ɋz��adsorption�Ɨސ������j�A�t�ΐ͂͐��ʂ��ŗ�p���x�Ȃǂɕq���ł���B
�@�t�ΐ͂͑��x�ߒ��Ɠ��I���ۂɈˑ����A�_���ׁ\�n�������̗̂��E�ւ̊g�U�Ő�����B
�@�t�ΐ͉͂ߓn�I�ŁA��ʓI�ɂ����g�U�ߒ������S�ȕ��t�ɓ��B���邱�Ƃ��\�Ƃ���Ȃ�A���Ԃ������ɋ߂Â��ɂ�ď��ł���B
�@���t�ΐ͉͂t�ΐ͂ł��邪�t�ΐ͉͂t�ΐ͂Ƃ͈قȂ�B
�@�t�ΐ͂͏Ă�����i�}��j�Ő�����M�U�N�t�ΐ́A�����q��z�q�Ȃǂ̏Ǝ˂ɂ���Đ�������ː��Ǝ˗U�N�t�ΐ́A
��͂ł̒e���ό`�ɂ���͗U�N�t�ΐ́A�����ł̑Y���ό`�ɂ��ό`�U�N�t�ΐ͂�����B
�@�܂��ړ��E�ʂł̗n���ςݏd�ˁi�p�C���A�b�vpile-up�j�ł��t�ΐ͂͐�����B
�@�t�ΐ͂ł͋}��A���́A���ː��Ǝ˂ȂǂŁA�t�ȓ_��E����������A�����Ɨ��E�ł̋�E�̏��ł̂��₷���̈Ⴂ�����E�Z�x���������A
�n�����q�Ƌ�E�̑��ݍ�p�̌��ʁA���t�ΐ͂Ɣ�ח��E�̉��w�g���������I�ɕω�����B
�@���ː��Ǝ˗U�N�t�ΐ͂ł͋�E�̗��E�ւ̈ړ��ɂ���āA���E�ߖT�̍������̔C�ӂ̌��q���t�ɋ�E�T�C�g�Ɉړ����A���E�ߖT��
���̌��q�̌��R�܂��͑��̌��q�̕x����������t�J�[�P���h�[������inverse Kirkendall effect�Ȃǂ������ɐ��肳��Ă���B
���d�����Ɖ��Ɣ�d�����Ɖ�
�@�ፇ���\���|�̐Ɖ��͍d�����Ɖ��Ɣ�d�����Ɖ��ɕ�������B
�@�d�����Ɖ��͌ŗn�����A�͏o�����̂悤�ȍ������ɂ�鋭���ň����N�������B
�@��d�����Ɖ��͎�ɂo�A�r�Ȃǂ̕s�������f�̗��E�ΐ͂ɂ���Ď�Ɉ����N�������B
�@���̑�\�I�ȗႪ�ፇ���|�̏Ă��߂��Ɛ��ŁA��Ƀ����iP�j�̗��E�ΐ͂������ł���B
�@�܂�Fe��j�b�P���iNi�j�̍����ł͗����iS�j��P�������ɋ������E�Ɖ����N�������Ƃ��m���Ă���B
�@����獇���̐Ɖ��͍����ɂ�鋭�����N�������ɕs�����̕ΐ͂̑����ő��傷��B
�@����A�|�ł͂a�A�a���A�l���Ȃǂ̂������̌��f�̗��E�ΐ͂͗��E�̋��x�����コ����B
���E�ΐ�desegregation
�@���q�̕��z�i�Z�x�j���������炷���q�̈ړ���ΐ�segregation�Ƃ����ꍇ�A���q�̕��z�����������錴�q�̈ړ���E�ΐ͂Ƃ����B
�@�����悤�Ȍ��t�ɋt�ΐ͂Ƃ��������������邪�A����͐���ΐ͂ɂ����錴�q�̕��z�ƈقȂ�Ȃ�ΐ͂̂�����i���q�̕��z�j�������̂ł���B
�i�P�P�j�@�M����
�i�P�P�|�P�j�@�M����
�@�����ł͎�X�̖ړI�̂��ƂɎ�X�̔M�����i���鉷�x�ł̉��M�j���s����B
�@�|�ł͍d���}���e���T�C�g�邽�߂̏Ă�����quenching�ƏĂ�����ɂ��d���ĐƂ��g�D�ɐx����^����
���߂̏Ă��߂�tempering����\�I�ł���B
�@���̂ق��������̑傫����`��𐧌䂷��Ă��Ȃ炵normalizing�i�ď��j�A�ΐ͂�����������A���H�d���E���H
�c������������A�Y������������A��퐫�����コ����Ȃǂ�ړI�Ƃ���Ă��݂�annealing�i�ē݁j�Ȃǂ�����B
�i�P�P�|�Q�j�@�|�̓����i�P���j�ϑ�isothermal transformation
�@�|���I�[�X�e�i�C�g�����ϑԓ_���x�ȉ��ɗ�p���Ă̈�艷�x�ł̕ϑԂ��i�P���j�ϑԂƂ����B
�@���x�������ق�����p�[���C�g�i�`�T�T�O���t�߁j�A�x�C�i�C�g�A�}���e���T�C�g��������B
�@�I�[�X�e���p�[�̓x�C�i�C�g�̈�ɏĂ����ꂵ�x�C�i�C�g�g�D��A�}���e���p�[�̓}���e���T�C�g
�ϑԊJ�n���xMs�ȉ��̔M���ɏĂ����ꂵ�c���I�[�X�e�i�C�g�̍P���ϑԂ��s���Ă��߂��}���e���T�C�g��
�ቷ�x�C�i�C�g�����g�D�Ƃ���A�}���N�F���`��Ms�_����̉��x�ɏĂ�����ێ��������̉��x������������
�����₵���X�Ƀ}���e���T�C�g�ϑԂ�������B
�E�s�s�s Time-Temperature-Transformation�Ȑ��i�r�Ȑ��j�F�P���ϑԋȐ�
�@�@�I�[�X�e�i�C�g������̉��x�ɏĂ����ꂵ�A���̉��x�ŕێ������Ƃ��̑g�D�������B
�@�@�r����������̂łr�r�Ȑ��Ƃ������A�o��������������@Nose�i���邢�͕GKnee�j�Ə̂��A�������̓p�[���C�g
�@�ϑԂŁA���̓x�C�i�C�g�ϑԁB
�E�b�b�scontinuous-Cooling-Transformation�Ȑ��F�A����p�ϑԋȐ�
�@�@���̗�p���x�ŗ�p�����Ƃ��̑g�D�������B
�@

�i�P�P�|�R�j�@�@���H�M����
�@���H�ƔM�����̑g�ݍ��킹�ō|�̋����A�x�������s���B
�@��\�I�Ȃ̂̓I�[�X�t�H�[�~���O�ŃI�[�X�e�i�C�g��Ms�_�ȏ�̉��x�ʼn��H�����̂��}���e���T�C�g�ϑԂ�
�N��������B
�@�p�e���e�B���O�̓p�[���C�g�܂��̓x�C�i�C�g�g�D������Ԑ��������H���s���B
�i�P�Q�j�@�����̋����E�d��
�i�P�Q�|�P�j�@���H�d��
�@�]�ʖ��x�̑����ɂ����̂�
�@�@�@�x�C���[�E�n�[�V��Bailey-Hirsch�̊W������B�ՊE����f���̓т�
�@�@�@�с����ʂ����P�^�Q�@�@�@�@���F�萔�A�ʁF�������A���F�o�[�K�[�X�x�N�g���̑傫���A�ρF�]�ʖ��x
�@�@�@������P�^�Q
������������substructure hardening,
�@���X�p���E�i�������ʍ��P�T�x�ȉ��j���������Ƃ��āAHall-Petch�̍l�������K�p�ł���Ƃ��A���̈��������ɂ��
�ɂ�鋭�������H�d���Ƃ͕ʂɈ����������Ƃ���l��������B
���ĕt�d��bake hardening�@�@
�@�@�@�R�b�g�������͋C�̌`���i�Ђ��ݍd���j�Ɠ]�ʏ�ւ̐͏o���`���i�͏o�d���j�̂Q�i�K�̍d���B
�@�@�@���邢�͉��H�d���ƂЂ��ݎ����d���i�ĕt�d���j�̗��p�B
�@�@�@�b�A�m�̉e�������������|�i�b�C�m���������A���邢�͒Y�����`�����f�ŌŒ�j
�@

�i�P�Q�|�Q�j�@��������������
�@�����̋��x�Ђƌ������a���ɂ̓z�[���E�y�b�`Hall-Petch�̊W
�@�@�@�Ё����O�{�����|�P�^�Q�@�@�@���O�A���͒萔
��������B
�@�������a���������Ȃ�Ɓi�P�Onm���x�j�ŋt�ɋ��x���������Ȃ�tHall-Petch�̊W��������Ƃ�������B
�@���I�A���Č�������悤�ȋ����Hsevere plastic deformation�ɂ��P�ʂ��ȉ��̌������������\�ŁA���̂悤��
�����H���@�Ƃ��Ăg�o�s�i�������˂���j�A�`�q�a�i�J��Ԃ��d�ːڍ������j�A�d�b�o�`�i���f�ʌX�Ίp�����o���j�Ȃǂ���������Ă���B
�@�����̍������ɂ�鋭���E�d���ɂ͈ȉ��̂R�^�C�v������B
�i�P�Q�|�R�j�@�ŗn����
�@�ŗn�̌`���ɂ�鋭���łb�������i�b���|�y���A�b���|�r���Ȃǁj���L���B
�@�u���^�ƐN���^������B
�@�ŗn�����ł�
�@�@�ՊE����f���́�i�ŗn�Z�x�j����
�@�@�ŗn�̂ł́@�@�@�����P�^�Q�@�iFriedel���E�j
�@�@���Z�x�ŗn�̂ł� �@�����Q�^�R�@�iLabusch���E�j
�����Ă͂܂�Ƃ����B
�i�P�Q�|�S�j�@�͏o�����i�����j
�@�`���|�b���������L���ʼnߖO�a�ŗn�̂���̋����ԉ������̐͏o�i�����j�ɂ��B
�@�e���ł͒Y�����A�������̐͏o�ōd�����N����B
�@�͏o�����ł�
�@�@�ՊE����f���́���R�^�Q�i�����j�P�^�Q�@�iGerold��Haberkorn�j�@�@�ÁF�i�q�萔�̃~�X�t�B�b�g��
�@�������͏o���͕��U���q��菬�������ߓ]�ʂ̈ړ��ɑ��ア��Q���i�]�ʂɃJ�b�e�B���O�@�\�������j�Ƃ��ē���
�@�͏o���̑����ŏ�Q�̎コ��₤�K�v������B
�@�͏o�����̋@�\
�@�@���w����chemical strengthening
�@�@�@�V�\�ʌ`���ɂ��E�ʃG�l���M�[�̉e��
�@�@��������modulus
�@�@�@�e�����̍��ɂ��
�@�@�������Ђ�����coherency strain
�@�@�@�������͏o�����ӂ̉��͏�Ɠ]�ʂ̒e�����ݍ�p
�@�@���q�K������order
�@�@�@���ʑ��E�ʂ̌`��
�@�@�ϑw������stacking fault
�@�@�@�ϑw���׃G�l���M�[���̉e��
������aging
�@�@�����̐����i�d�C��R�A�d�x�A���x�Ȃǁj�����Ԃ̌o�߂ƂƂ��ɕω����邱�ƁB
�@�@�����d���͐͏o�d���ɂ��B
�@�@���R�����i�퉷�����j�Ɛl�H�����i�Ă��߂������j������B
�@�ߎ���overaging�@�@
�@�@�d�x�A���x�Ȃǂ��ō��ɂȂ鉷�x�A���Ԃ����������x�A�������x�ł̎����ōd�x�A���x��
�@�Ăђቺ���錸���B�����ɂ���ď㏸�����d�x�A���x���Ăь�������ꍇ�B
�@�@����ɑ��d�x�A���x���ō��ɂȂ�O���ߏ������i�s���S�����junderaging�Ƃ����B
�@�@���������̐͏o�����������Ƃ��͓]�ʂ����q��ؒf����J�b�e�B���O�@�\�i���q����f�@�\�j��
�@�x�z���~�����̓т͗��q�a���Ƒ̐ϕ������ɑ�
�@�@�@�с�(f��)1/2
�@�@���q���d���قǁA�ꑊ�̌����i�q�Ɛ������������قǁA�~�����͂͑傫���Ȃ�B
�@�@�͏o�������������q�ԋ������傫���Ȃ�Ɠ]�ʂ͐͏o�����I�ē]�ʃ��[�v���`������
�@�I�������@�\���x�z��
�@�@�@�с�f1/2��-1
�@�@���q�̐����ɂ͊W���Ȃ��B
�@

�@����reversion�@�@
�@�@�@�����d�������Ŏ������x��荂�����x�Ŏ����O�̐����ɖ߂�A����錻�ۂŁA�d���̌���
�@�@�ł������͏o���̍Čŗn�ɂ��N����B
�@�Ђ��ݎ���strain aging
�@�@�ÓI�Ђ��ݎ���static
�@�@�@�@��ԑY�����H���s���Ɖ��H�d�����N�������A���H��̎��Ԃ̌o�߂ƂƂ��ɍd�����i�s����
�@�@�@�ꍇ��ÓI�Ђ��ݎ����Ƃ����B
�@
�@�@���I�Ђ��ݎ���dynamic
�@�@�@�@���ԉ��H���ɉ��H�d���i�~�����͏㏸�j���N���錻�ۂI�Ђ��ݎ����Ƃ����B
�@�@�K���ȉ��x�ŋ��n��i�s�A���A�Z���[�V�����A���͐U���j�̉��́|�Ђ��ݐ��}���邱�Ƃ��m���Ă���A
�@������|���g���@���E���V���g���G�iPortevin-LeChatelier�j���ʂƂ����B
�@�@���̌��ۂ͗n�����q�Ɠ]�ʂ̑��ݍ�p�iCottrell�Œ��j�ɋN�����铮�I�Ђ��ݎ����Ƃ��邱�Ƃ�����B
�@�@

�@���͎���stress aging
�@�@�@���̋@�B�I���͂ƔM���ɉ����C��莞�ԕێ�������H�M�����B
�@�@�@�O�͂�t�����Ă̎����B
�i�P�Q�|�T�j�@�ϑԍd��
�@�e���|�b�̃}���e���T�C�g�ϑԂ�����B
�@�͏o�����ƕ����I�ɂ͓������������@�\���قȂ���̂ɕ��U����������B�͏o�������L���Ӗ��ł͕��U�����ł���B
�i�P�Q�|�U�j�@���U����
�@�d�����đϔM���̂���Z���~�b�N���q���Ɏ_�����Ȃǂ���݂�����B
�@�_�������U����Oxide Dispersion Strengthened �n�c�r�����Ȃǂ�����B
�@��Ƃ���SAP�iSintered Aluminum Poweder�AAl����Al2O3�j�A�A���~�i���U�������A�n�c�r��i�b���n�ASnO2�Ȃǁj�A�n�c�r�iZrO2�j�����A
�@�s�c Thoria Dispersed�j�b�P���iThO2�j�AODS�iY2O3�Ȃǁj�m��������A�n�c�r�iY2O3�Ȃǁj�t�F���C�g�|
�@�͏o�����͗n�̉��E�����ɂ�邪���U�����͗n�������̑I���_���i�����_���@�j�|�M�����A��������@�iMA���J�j�J���E
�A���C�@�i�������m���{�[���E�~�������j�ȂǁA�j�|�ϔM�����A�ȂǂŐ����B
�@���U�����ɂ�Zener�̎����K�p�����B
�@�@�@�q���j���^���@�@�q�F�������a�A���F���U���q�a�A���F���U���q�̐ϗ�
�@���U�����ł�
�@�@�ՊE����f���́�ゆ�^���@�@
�@���������U���q�͑傫���I�������@�\�i���[�v�@�\�A�o�C�p�X�@�\�j�������Ƃ���B
�@�J�b�e�B���O�@�\�ƃI�������@�\�̗ՊE���a�͐������`���\�����ł���B
�i�P�Q�|�V�j�X�s�m�[�_�������ƋK���i�q�`��
�E�X�s�m�[�_�������ɂ�鋭��
�@�@�Z�x�ϒ��̐U���ɔ�Ⴕ�g���ɂ͖��W�B�b���|�m���|�r���n�����Ō�����B
�E�K�����d��
�@�@�`���b�������i���ȗp�����j�ł͋K���i�q�`���ɂ��d����������B
���W���g�D�d��texture hardening
�@�@�s������������}�O�l�V�E�������A�y���A�a���Ȃ��f���Z�����\���ł͂��ׂ��������ʏ�ɑ��݂��A
�@��ʏW���g�D�����Ŕ������̕ό`������ƂȂ�ʓ��Q�����͏�Ԃł̋��x�������Ȃ�B
�i�P�R�j�@���ϑԂ̎�ށE����
�@���ϑԂ��邢�͑��]�ڂƂ��������������邪�Ⴂ�͂��邩�B
�@�@���ϑ�phase transformation�E�E�E�L���X�y�N�g�����̌��ہB
�@�@���]��phase transition�E�E�E���ꉻ�w�g���̂Q���Ԃ̓]�ځB
�@�@������phase reaction�E�E�E��Q���̐͏o�i���L�����{���j�A���́i�������{���j�Ȃǂ͉��w�ł͑������B
�@�Ƃ����l������B
�@�@�@
�i�P�R�|�P�j�M�͊wthermodynamic�I����
�i�P�R�|�P�|�P�jEhrenfest�̕���
�@�@�@�@���]�ڂ̎������M�b�u�X�̎��R�G�l���M�[�̓���
�@�@�@�@�@�@�P�����]�ځF�P���������[���łȂ��A�L���i�G���g���s�[�ω����O�j�A�Q�������͖����i�b�������j�B
�@�@�@�@�@�@�@�@�@�@�@�@�G���g���s�[�A�G���^���s�[�i�����M�j�A��̐ς̕s�A���ω�
�@�@�@�@�@�@�@�@�@�@�@�@
�@�@�@�@�@�@�Q�����]�ځF�P���������[���A�Q�������͗L��
�@�@�@�@�@�@�@�@�@�@�@�@�G���g���s�[�A�G���^���s�[�A��̐ς̘A���ω�
�@�@�@�@�@�@�������]�ځF�����������L�����s�A��
�@�@�@�@

��Ubbelohde�̕���
�@�@�@�@�@�i�M�͊w�I�j�A���i�s���āj���]�ځ@�@
�@�@�@�@�@�@�@�@�@�@�G���^���s�[�̕s�A�����Ȃ��B�����\���ω����~���ŘA���I�B
�@�@�@�@�@�i�M�͊w�I�j�s�A�����]�ځ@
�@�@�@�@�@�@�@�@�@�@�Q���̍\�������ɂ͂�����ƈقȂ�~���ɕω��ł��Ȃ��B
�@�@�@�@�@�@�@�@�@�@�Ήp�[�N���X�g�o���C�g�A�_�C�A�����h�[�O���t�@�C�g�B
�@�@�@�@�����͓����I�ُ팻�ۂ�悷��B
�@�@�@�@�@�s�A�����]��
�@�@�@�@�@�@�@�@�v���]�ڂ���уv���n�Z���ہA����͗ގ���ނ̌����̒i�K�Igradual�\���ω��ɂ��B�i���������j
�@�@�@�@�@�s���ĂȂ����A�����]��
�@�@�@�@�@�@�@�@�����̓]�ڂɂ��Ƃ���邱�Ƃ�����B�����P�ꌋ�����̂Q�̂킸���ɈقȂ�\���Ȃ����T�u�P�ʗ̈�̋����ɂ��B
�@�@�@�@�@�@�@�@�M�͊w�I�]�ړ_�ł̃q�X�e���V�X�̔����B����͕s���ĔM�͊w�]�ڂ������炷�������ۂ��琶����B
�i�P�R�|�P�|�Q�j�����_�E�̌��ۘ_
�@�@�]�ډ��x�ߖT�Ŏ��R�G�l���M�[�𒁏��ϐ��i���ʕϐ��j�œW�J�A�����̑Ώ̐����l���B
�@�@�@�@���R�G�l���M�[�𒁏��p�����[�^�[�řp��W�J�@�@���f���`�łQ�{�a�łR�{�b�łS�E�E�E
�@�@�@�@�@�@�P���@�a���n
�@�@�@�@�@�@�Q���@�����p�������A��p���Ȃ��B�a���O
�@�@�ꎟ���]�ڂƓ��]��
�@�@�@�@�ꎟ���]�ځF�]�ډ��x�Œ����ϐ����s�A���I�ɂO�A���M�̔����B
�@�@�@�@���]�ځF�]�ډ��x�Œ����ϐ����A���I�ɂO�A�������̔��U�B
�@�@

�@�@�@�����ϐ��F���]�ڂ��L�q���鎦�ʕϐ��i�傫�����̐ςɔ��j�B
�@�@�@�@�@�@�@�@�@�@�]�ډ��x�ȏ�i���������j�ł͂O�ŁA�ȉ��i�������j�ł͂O�łȂ��l�B
�@�@�@�������F�����ϐ��̓����B
�@�@�@�ՊE�w��
�@�@�@�@�@�������A�������A�����Ȑ��A������M������t����w���i�X�P�[�����O���j�B
�@�@�@�@�@�X�P�[�����O���ƃ��j�o�[�T���e�B�i�w���Ԃ̊W�j�B
�@�@�@�ՊE����
�@�@�@�@�@�����_�E���_���Ȃ肽���Ȃ����ہA���邢�͗̈�i�ՊE�̈�j
�i�P�R�|�P�|�R�j�Ώ̐��j��]�ڂƑΏ̐��ۑ��]��
�E�h�t�o�`�b�̒�`
�@�@�E�Ώ̐��ۑ�conserving�]��
�@�@�@�@����̑��̃Z�������܂��́A����ъp�x�������ƈقȂ邪��ԌQ�Ώ̐��͕ۑ��A��G�������b���̗�p�ɂ��P�O�������x���������]��
�@�@�@�i�C�́|�t�́j
�@�@�E�Ώ̐��j��]�ځi��sub�O���[�v�|��super�O���[�v�]�ځF�j
�@�@�@�@��Ώ̑��̋�ԌQ�Ώ̐������Ώ̑��̈��O���[�v�A��G�ቷ�Ήp�i�o�R�P�Q�F�O�j�ƍ����Ήp�i�o�U�Q�Q�Q�F�Z���j
�@���邢��
�@�@�ψʑ��]��
�@�@�@�@���]�ڑO��̑Ώ̌Q�̓O���[�v�E�T�u�O���[�v�W������
�@�@�č\�����]��
�@�@�@�@���]�ڑO��̑Ώ̌Q�̓O���[�v�E�T�u�O���[�v�W�������Ȃ�
�i�P�R�|�P�|�S�j���萫�ɂ�镪��
�E�t�E�s�t
�@�@�@�@�ݕ�enantiotropic�]�ځE�E�E�t�i���t�]�ځj
�@�@�@�@�P��monotropic�]�ځE�E�E�s�t
�E����E������
�@�@�@�@������@
�@�@�@�@�@�@�P�����]��
�@�@�@�@�@�@�@���R�G�l���M�[�Ȑ��̊O�}�A�������ԑ��݁B
�@�@�@�@�@�@�Q�����]��
�@�@�@�@�@�@�@���R�G�l���M�[�Ȑ��͘A���Ȑ��ŏ������Ԃ̊T�O���݂����B
�@�@�@�@����
�@�@�@
�@�@

��������Ɣt
�@�E��������
�@�@�@�@�߁i���j�M
�@�@�@�@�ߗ�p
�@�@�@�@�ߖO�a
�@�@�@�����葊
�@�@�@�@���t�����X�A�p��̃E�B�L�ł͑��x�_����A�h�C�c��A���{��͂������̑召�i�G�l���M�[��ǂ̑傫���j
�@�@�@�@���I�X�g�����g�̒i�K��
�@�@�@�@�@�@�@�ߖO�a�t�̂���ŏ��ɐ�������鑊�͕K�������M�͊w�I�Ɉ���ȑ��ł͂Ȃ��A�t�̂ƃG�l���M�[�̋߂����ł���B
�@�E�t�̕��t
�@�@�@�@�t��Ԃ́i���������Ȃ��Ă��j���Ԃ������ĕ��t��Ԃ�
�@�@�@�@�������t�i���ÓI�j
�@�E�n�̔M�͊w�I����
�@�@�@���t
�@�@�@�@����
�@�@�@�@������
�@�@�@�@�s����
�@�@�@�t
�@�@�@�@�@�n���̔M�͊w�I�ψ�i�ɘa���ہj
�@�@�@�@�@�@�@�@���^�A����^
�@�@�@�@�@�n���̔M�͊w�I�s�ψ�i�A�����ہj
�@�@�@�@�@�@�@�@���^�A����^�A���A����
�@�@���ߗ�p�t�̂͏����蕽�t�ŃK���X�͔t������Ԃ����K���X��t�����ԂƂ��̂��邱�Ƃ������B
�@�@�@�@
�i�P�R�|�Q�j�@�\�Imechanistic����
�i�P�R�|�Q�|�P�jGibbs�̍l��
�@�@�@�@��炬fluctuation�����ƂƂ���
�@�@�@�@�V���`���ߒ�
�@�@�@�@�@�A�����]�ځE�E�E�傫�ȋ�Ԃŏ����ȑg���h�炬�Ŏn�܂�@�@���X�s�m�[�_������
�@�@�@�@�@�s�A�����]�ځE�E�E�����ȋ�Ԃő傫�ȑg���h�炬�Ŏn�܂�@�@���j�����E����
�i�P�R�|�Q�|�Q�jChristian�̕���
�@�E����homogeneous���ϑ�
�@�@�@�@�@�A���A�j�������Ȃ�
�@�@�@�@�@�X�s�m�[�_�������A�`���|�b���̃X�s�m�[�_���K����
�@�E�َ�heterogeneous���ϑ�
�@�@�@�@�@�s�A���A �͂����肵���E�ʁA�j�����Ɛ���
�@�@�@�@�@�`���|�b���K����
�@�@�@��Cellular��͏o�Ƌ��͏o
�@�@�@�@�@�@Cellular��͏o�i�s�A���͏o�j
�@�@�@�@�@�@�@���f�����{��
�@�@�@�@�@�@����
�@�@�@�@�@�@�@�������{��
�@�@

�@�@�@Christian�̕���
�i�P�R�|�Q�|�R�jBuerger
�@�@�@�@�z�ʐ��ƌ����^�ɂ�镪��
�@�@�@�@Reconstructive�icivilian�j��Displacive�imilitary�j
| �]�ڂ̌^ | �� |
| �P�D��P�z��coordination���܂ޓ]�� | |
| �i���j�č\��Reconstructive�i�x���j | �_�C�A�����h�̃O���t�@�C�g |
| �i���j�c��Dilational�i�����j | �≖�̂b���b�� |
| �Q�D��Q�z�ʂ��܂ޓ]�� | |
| �i���j�č\��Reconstructive�i�x���j | �Ήp�̃N���X�g�o���C�g |
| �i���j�ψ�Displacive�@�@�@�@�@�i�����j | �ቷ�̍����Ήp |
| �R�D�s�K��disorder���܂ޓ]�� | |
| �i���j�u��Sustitutional�i�x���j | �ቷ�̍���LiFeO2 |
| �i���j�z��Orientational �@�@�@��]Rotational�@�@�@�@�@�i�����j |
���U�d�́̏�U�d��NH4H2PO4 |
| �S�D�����^�̓]�ځ@�@�@�@�@�@�i�x���j | ���i�D�j�̃��i���j�r�� |

�@���ϑԂ̓���
| �ϑԂ̌^ | ���� |
| �ψʌ^���ϑ� | �����̏����ȕό`�i�c�����邢�͉�]�j�Ői�s�B ���q�ψʂ͂O�D�O�P�|�O�D�P���B ���ԂɃO���[�v�|�T�u�O���[�v�W������B �P���܂��͂Q���̑��ϑԁB |
| �č\���^���ϑ� | �P�����邢�͂Q���̌����j��ɂ���Đi�s�B �P�O�|�Q�O���̊i�q�ό`�̑傫�Ȍ��q�ψʁB �G�l���M�[��ǂ������̕ϑԂ͒x���B ���ԂɃO���[�v�|�T�u�O���[�v�W���Ȃ��B �ϑԂō������̑Ώ̐��������Ȃ�B |
| �K���E�s�K���^ | ���q�u���Ői�s�A���炭�����Ȍ��q�ψʂ��B �b���y���ł̓O���[�v�E�T�u�O���[�v�W��ێ��B �`���A�e���A�b���A�y���r�A�r���b�i�e�b�b�|�g�b�o�j�͍č\���I�B |
�i�P�R�|�Q�|�S�jCohen�̕���
�@�@

�E�i�q�ό`�ϑ�

�E�V���b�t���ϑ�


�@�@�@�@�@�@�@�@�@�@�@�@�֑��@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�r���s���n�R
�i�P�R�|�Q�|�T�jDelaey�̋����̑��ϑԂ̕���
�@

�@
��Rao�ɂ������n�̑��ϑԂ̊W

�������t�H�g���s�b�Nmorphotropic�ϑԁi���`���ϑԁA�������ϑԁA�g�����ϑԁj�@�@
�@�@�ŗn�̂ł̑g���ω��ɂ�鑊�ϑԁB���̑g���͉��x�ɂ��ω����ɂ����B
�@�@���̑��ϑԂ̋��E�������t�H�g���s�b�N�����E�l�o�a�Ƃ����B
�@�@�o���y���n�R�|�o���s���n�R�n�ł͐������ƕH�ʑ̏��̂l�o�a�t�߂ň��d���̗D�ꂽ�������������邱�ƂŗL���B
�@

���\�����]�ځ@
�@�@�@���q�̊g�U��Ȃ������\���̂킸���ȕω��ɂ��ő��Ԃ̑��]�ځB
�@�@�@��������ቷ�őΏ̐��̒ቺ��������B���q�̋ɂ߂Ă킸���Ȉړ��őΏ̐����ω��B
�@�@�@�����]�ڂ��N�����A���邢�͓���̌����\�����Ƃ錴�q�Ԃ̑��ݍ�p�͉����B
�@�@�@ �����|�������^
�@�@�@�@�@���q�͋�ԓI�ɗ��U�I�ȓ�ȏ�̈���ʒu�̑���
�@�@�@�@�@�C�W���O�X�s���ϐ��̒����ߒ�
�@�@�@�@�@�m���m�n�R
�@�@�@�@�@
�@�@�@ �ψʌ^
�@�@�@�@�@��ԓI�ɘA���I�Ȍ��q�ψʂ̗h�炬
�@�@�@�@�@����t�H�m�����[�h�i�\�t�g�t�H�m���j�̕s���萫�A�Ώ̐��̍����ʒu�̎���ŐU�����Ă������q���Ώ̐��̒Ⴂ
�@�@�@�@�ʒu�œ����B
�@�@�@�@�@���w�I�t�H�m���̓����@���U�d��
�@�@�@�@�@�����w�I�t�H�m���̓����@���e����
�@�@�@�@�@���[�h�\�t�g���̌���
�@�@�@�@�@�@�@�i�q�U���̔a���A���̑��E�E�E
�@�@�@�i�����^�j
�@�@�@�@�@�C�W���O�X�s���|�t�H�m�������^
�@�@�@�@�@�@�@�m�g�S�a��
�@�@�@�@�@�d�q�n�|�t�H�m�������^�@
�@�@�@�@�@�@�@���[���E�e���[����
�@�@�@�������
�@�@�@�@�@���q�ԁA���q�Ԃ̑��ݍ�p�i�C�W���O�X�s���A�t�H�m���j���ɒ[�Ɉٕ���
�@���\�t�g�t�H�m���@
�@�@�@�ψʌ^�̋��U�d�̂ł͏�U�d���̐ԊO�����i�q�U�����[�h�Ɏ��g���̔��ɒႢ���́i�\�t�g�E���[�h�j
�@�@�����݂��A�]�ړ_�ɋ߂Â��ƐU�������X�Ɍ������A���̐U�������債�₪�ĐU�������������]�ڂ��N�����
�@�@���߂����B
�i�P�R�|�Q�|�U�j��vcongruent�ϑԁ̕���incongruent�ϑ�
�@�@�@��vcongruent�ϑԁ@�@����v�n�Z�A�ŗn�̂ł̋ɒl�i�t�����A�ő����̈�v�_�j
�@�@�@����incongruent�ϑԁ@������n�Z
�i�P�R�|�R�j���x�_kinetic�ɂ�镪��
�i�P�R�|�R�|�P�jLe Chatelier�̕���
�@�@�@�@�}��rapid�܂��͔�ē��ꐫnonquenchable�@�E�E��M����athermal
�@�@�@�@�ɖ�sluggish�܂��͏ē��ꐫquenchable�@�@�@�E�E�M����thermal
�@�@�@�@�@�@����`�̞B����
�i�P�R�|�S�j�R�����I����
�i�P�R�|�S�|�P�jRoy�̕���
�@�@���x�_�A�M�͊w�ƔM���w�A�\��
�@

�@�@Roy�̕���
�@�@
�i�P�R�|�S�|�Q�jRao�̕���
�@�@�@�@�\�i�\���j�A�M�͊w�A���x�_�łR�����I����
�@�@�@�@�����@�@�\
�@�@�@�@�@�g�U�i�č\���j�@�͏o�A�A�����t�@�X�E�������ϑԁA�}�b�V�u�ϑԁA���͑�����
�@�@�@�@�@�ψʁ@�@
�@�@�@�@�@�@�@�i�q�Ђ��݁@�}���e���T�C�g�ϑ�
�@�@�@�@�@�@�@�V���b�t���@�@�֓]�ځA���U�d�̓]��
�@�@�@�@�@����
�@�@�@�����@�M�͊w
�@�@�@�@�@�P���@��̐ρA�G���^���s�[�A�G���g���s�[�̕s�A���ω�
�@�@�@�@�@�����@�A���ω�
�@�@�@�@�@����
�@�@�@����
�@�@�@�@�@�M����thermal�@�@�ψ�
�@�@�@�@�@��M����athermal�@�@�č\���i�g�U�j
�@�@

�@Rao�ɂ�鑊�ϑԂ̕���
�@
�i�P�R�|�T�j����ȑ��]��
�T�|�P�j�ÓT�I���]�ڂƗʎq���]��
�E�ÓT�I���]��
�@�@�@�M�h�炬�ɂ���Đ�����B���x�㏸�ɂ��G���g���s�[���傪�����B�ቷ�̍����������獂���̒ᒁ�����ւ̕ω��B
�E�ʎq���]��
�@�@�@��Η�x�ł̗ʎq�h�炬�i�s�m�茴���ɂ��j�ɂ�钁�����Ɨʎq���������ւ̑��]�ځB
�@�@�@���́A���ꓙ�������ŋN����B
���g�|���W�J��topological���]��
�@�@�@�g�|���W�J�����ׁi�Q�A��ʂȂǁj�̋Ïk�ł�����B
�@�@�@�������̒��ԕψʒi�K�ɂ���ĉ��z�I�ȋO�Ղ��\������鋤���I�����I�K�̓W�����v�Ő�����B
�i�P�S�j�@��X�ȋ���
�i�P�S�|�P�j�@�o���t���[�͂i�����͂j
�@�����̐ڍ��Z�p�ŗn��welding�Ƃ͐ڍ����镔�ނڗn�Z�����Đڍ���������@�ł���ɑ��A�ڍ����镔�ނ���Z�_�̍�����
�ڍ����镔�ނɉ�݂����Đڍ����镔�ނ�n�Z�����Ȃ��Őڍ�������@�̂����S�T�O���ȏ���낤�t��brazing�Ƃ����A����Ɏg�p����
�ڍ����ނ��낤�i���邢�͍d�낤�j�Ə̂���B
�@�S�T�O���ȉ����͂t��soldering�Ƃ����A����Ɏg�p����ڍ����ނ��͂Ə̂���B
�@�]���͂t���ɂ͍L���r���|�o�������i�����j�n���g�p����Ă����B
�@�r���|�R�W�o���̋����g���́h�����͂h�ƌĂ�܂��r���|�S�O�o���₱���ɂ`����Y���ɋ����������̂Ȃǂ��g�p����Ă����B
�@���̂r���|�o���͍͂��������������i�o�����ΐ́A�e�剻���ΐ͕�����j��Ɏ���j�����ꂽ�͂����������Ă�����
���̓Ő��̂��ߎg�p�֎~�ƂȂ�o�����܂܂Ȃ��o���t���[�͂i�����͂j���g�p�����悤�ɂȂ����B
�@�����ŗZ�_�ŒႢ�̂͂h���i�P�T�V���j�A�r���i�Q�R�Q���j�A�a���i�Q�V�P���j�A�b���i�R�Q�P���j�A�o���i�R�Q�W���j�Ȃǂł��邪�A�o���t���[�͂�
�̌��ƂȂ����̂͂r������b�Ƃ��鋤���n�łr���|�`���A�r���|�b���A�r���|�a���A�r���|�y���A�r���|�h���Ȃǂł���B
�@�Z�_�ȊO�ɋ�����ׂ������͔G��L����A�όE�ϐH���A�@�B�I�����A���H���A�R�X�g�Ȃǂł���B
�@�r�������ɂ͉��������`��������̂Ƃ��Ȃ����̂�����B�@�@
�@
�@�����`���r�������n
�@�@�r���|�X�y���@
�@�@�@�����_�P�X�W���A�r���ɂy���ŗn����i�P���������x�H�j�A���H�A�G��L����ɖ�肠��B
�@�@�@���ی������ꂽ�̂͂r���|�W�y���|�R�a���B
�@�@�r���|�T�V�a���@�@
�@�@�@�����_�P�R�X���A�r���ɂa���ŗn����i�P�������ȏ�j�A�@�B�I�����ɖ�肠��B
�@�@�@�r���|�T�V�a���|�P�`���ȂǁB
�@�@�r���|�O�D�T�`���@
�@�@�@�����_�Q�Q�W���A���H�A�G��L����ɖ�肠��B
�@�������`���r�������n�@�����ԉ��������̓t�@�Z�b�g�ƂȂ�B
�@�@�r���|�R�D�T�`���@�@
�@�@�@�����_�Q�Q�P���A�ŗn�ʂ͂O�D�P�������ȉ��B
�@�@�r���|�O�D�V�b���@�@
�@�@�@�����_�Q�Q�V���B
�@�@�r���|�T�Q�h���@�@�@
�@�@�@�����_�P�P�W���A�h�������A����Ԃɕs������B
�@�@�r���|�P�O�`���@�@
�@�@�@�����_�Q�P�V���A�`�������叻�Ƃ��ď��o����������
�@�@�r���|�Q�l���@
�@�@�@�����_�Q�O�O���@
�@�@��ʂɋ��x����̂��߂`���A�G�ꐫ����̂��߂a���A�Z�_��̂��߉��a���A�h���Ȃǂ��Y�������ꍇ������B
�@�@�m���A�b���A�e���Y���͂قƂ�ǗZ�_������Ȃ�����R�����Ƃ��ēY�����邱�Ƃőg�D���P�Ɍ��ʂ�����B
�@�@�_���}���ɂo�A�f���̓Y�����s�Ȃ���ꍇ������B
�@�R���n
�@�@�r���|�`���|�b���@�@
�@�@�@�����_�Q�P�V���A�R�D�T�`���|�O�D�X�b�����č������W���Z�p�������m�h�r�s�ɂ������B
�@�@�r���|�b���|�b���@
�@�@�@�r���|�O�D�U�W�b���|�O�D�R�V�b���������g���ŋ����_�Q�Q�S�D�S���Ƃ����B
�@�͂t���œ��ɓd�q��H�Ŏg�p����ꍇ�A�ڍ����鑊��i�d�Ɂj�͎�ɂb���A�m���ł����͂r���Ƌ����ԉ��������`�����A
�r���̊����̑����o���t���[�͓͂��ɋ����ԉ��������������₷���j��͎�ɋ����ԉ������̕����ŋN����B
�������͂�
�@�K�w�͂t���i�p�b�P�[�W�̓����ł̓d�q�f�q�ƃp�b�P�[�W�̐ڍ��j�A���d�́i�p���[�j�n�����̃_�C�E�{���h�i�_�C�E�A�^�b�`�j�@
���Ȃ킿�_�C�͔����̃`�b�v�̂��ƂŁA���d���i�p���[�j�n�����̃`�b�v�Ƃ��̑�ƂȂ郊�[�h�E�t���[���̐ڍ����ɏ�L�͂��Z�_
�̍����͂����p�����B
�@�悭���p�����̂͂o���W�T���ȏ�̂r���|�o�������͂B
�@�@�P�O�r���@��Q�V�O���ȏ�
�@�@�@�T�r���@��R�O�O���ȏ�
�@�o���t���[�����͂��Ƃ��Ă�
�@�@�`���|�Q�O�r���@
�@�@�@�����_�Q�W�O���A�����ԉ��������u�̋����A�t���b�N�X���X�̃N���[���͂t���\�B�����B
�@�@�r���|�X�r���i�Ώ��j�@�@
�@�@�@�Ώ��_�Q�S�U���A���x�����������B
�@�_�C�{���h�i�_�C�E�{���f�B���O�j�p�Ƃ��Ă�
�@�@�`���|�P�Q�f���i�����_�R�T�U���j�A�`���|�R�D�P�T�r���i�����_�R�U�R���j�Ȃǂ����p����邱�Ƃ�����B
�@�X�Ɍ������ꂽ���̂�
�@�@�a���n
�@�@�@�a���|�Q�D�U�`���A�����_�Q�U�Q���A�@�B�I����������������B
�@�@�a���i�Q�V�P���j�|�r���i�U�R�O���j�n�A�S���ŗn
�@�@�y���|�`���n�@�@
�@�@�@�T�`���F�R�W�Q���A�����_�y���ւ̂`���ŗn��O�D�Q������
�@�@�@�y���|�`���|�l�����R���n���B�@
���낤��
�@�낤�ނ͂܂��G��L���萫���d�v�ł���A�܂��ϐH���A�ώ_������@�B�I�������d�v�ł���B
�@�����̓_����͈�ʓI�ɋM�������ǂ��B�܂������ԉ������̌`���͂Ȃ�ׂ�������ق����ǂ��B
�@��Z�_���̂��߂ɂ͂b���A�r���A�h���Ȃǂ̓Y�������ʂ����邪�b���͗L�Q�ŁA�r���Y���ł͗Z�_�͉����邪
�Ƃ��Ȃ錇�_������A����h���͐Ƃ��Ȃ錇�_�͏��Ȃ��������ł���B
�@�p�r�I�ɂ͋M�����A���ȗp�̐ڍ��Ɏ�ɋ��낤�i�`���|�`���|�b���|�y���n�A�R�O�|�V�O���`���A�j���g�p�����B
�@�H�Ɨp�ɂ͂`���|�b���n�i�W�O�`���ɂW�W�X���j�A�`���|�m���n�i�P�V�D�T�m���ɖ�X�T�O���j�����p�����B
�@���҂͋ɏ��Ȉ�v�n�Z���x�����B
�@�@

�@�@�@�@�@�`���|�m���n�Q����Ԑ}
�@���Z�_���̂��߂ɂ͂`���|�o���n�A�`���|�o���n�����p�����B�i����͂l���A�v�Ȃǁj
�@�o���͂b���A�`���A�`���A�m���ƑS���ŗn���A�G�ꂪ�ǂ��A�ϔM��������A�@�B�I�����͈������邱�Ƃ������A
�Ɖ����ɂ����̂ł����̑���ɂ悭�g�p�����B
�@�H�Ɨp�낤�ނ̒��S�ƂȂ��Ă���̂͂`���|�b���|�y���n����Ƃ����낤�ł���B
�@�`���|�b���Q�������̂`���|�Q�W�D�P�b���̋����V�V�X������b�Ƃ��A�y���͑����Ƃ`���Ƌ����ԉ��������`������
�̂łR�T���ȉ��ł���B
�@���Z�_�p�ɂ͂`���|�o���n���悭�g�p�����B�i�����y�[�X�g�p�j
�@

�@�@�@�@�`���|�b���|�y���R���n��Ԑ}
�@�@

�@�@�@�`���|�b���|�r���n�R����Ԑ}
�@

�@�@�@�`���|�b���|�h���n�R����Ԑ}
�i�P�S�|�Q�j�@�o���t���[����ށi��������ށj
�@����ނɂ͐���������A�H������̗ǂ��A�؍�\�ʑe���̏����Ȃ��Ƃ��v������A���Ɏ����@�ɂ��A�����H�̂���
����͍H��ɗ��܂��������������A��������������߂���B
�@���̂��߂ɂ͗n�Z�Ɖ����ʁA���͏W�����ʁA�������ʁA�H��ی���ʂȂǂ��������A�������U������B
�@�S�|�ł�
�@�@��Z�_�������U�^�F�o���A�a���A�i�r���j�ȂǂU�A�n�Z�Ɖ����ʁA�������ʁA�o���͓��ɋ@�B�I�����Ɖ��퐫���ǂ��B
�@�@���������U�^�F�l���r���U�A���͏W�����ʁA�������ʁA�@�B�I�����ٕ̈����傫���B
�@�@�`�䗰�������U�^�F�b���A�y���A�s�����邢�͂r���A�s���ŗ������̌`��E���z���P���@�B�I�����Ɖ��퐫�����P�B
�@�@�O���t�@�C�g�����U�^�F�O���t�@�C�g�A�Z�����a�m�ȂǂU�A���͏W�����ʁA�������ʁA����������B
�@�@��Z�_�_�������U�^�F�b���n�|�`���Q�n�R�|�r���n�Q�A�H��ی���ʁA�P�Ƃł͗��p����Ȃ��B
�@�@��̐Ɖ��^�F�����ԉ������A���������̐͏o�A�x���B
�Ȃǂ����p����邪�]���͓��ɂo������|�i�`�O�D�R���o���j���������p���ꂻ�̂ق��r����|�Ȃǂ����������A�o���t���[���ɂƂ��Ȃ�
�a������|�A�`�䗰��������|�A�a�m����|�Ȃǂ��J������Ă��邪�o������|�ɕC�G������͓̂����Ă��Ȃ��B
�@�`�������ł͂a����r����Y���������́A�����ł͂a����r����Y���������́i�����͏o�ɂ���̐Ɖ��j���J������Ă���B
�i�P�S�|�R�j�@�d�M�����A��R����
�d�M����
�@�@�����܂Ŏg�p�ł����R���M�p�����Ƃ��Ă̓j�N�����A�J���^���i�T���h���B�b�N�Гo�^���W�j���ǂ��m���Ă���B
�E�j�N�����i�j�b�P���E�N�����n�j�@�@�@Nikrothal�i�T���h���B�b�N�Ёj�ABrightray�iSpecial Metals Co.�j�ANicrofer�ACronifer�i�e�B�b�Z���E�N���b�v�Ёj�j�ȂǁB
�@�m���|�b���n�A�m���|�e���|�b���A�e���|�m���|�b���Ȃǂ�����P�`�Q�����x�̂r���A��y�ށi�k�����j�������ώ_���������コ���A�܂��P���O���
�l����Y�����ĉ��H�������P����B�e�b�b���i�I�[�X�e�i�C�g���j�����ł���B�b���Q�n�R�y�тr���n�Q�A�k�Q�n�R�Ȃǂ��ώ_���������コ����B
�@
�@�@�m���|�b���n�{�r���A��y�ށi�k�����j�@
�@�@�@�@�V�W�m���|�Q�O�b������\�I�B����͎_�����͋C�łP�Q�O�O���܂Ŏg�p�ł���B�퉷�ł̒�R�͂P�D�O�W�ʃ����A�P�S�O�O�������B
�@�@�@�@�U�W�m���|�R�O�b�����P�Q�T�O���܂Ŏg�p�ł��A�퉷�ł̒�R�͂P�D�P�W�ʃ����B
�@�@�m���|�e���|�b���{�r���A��y�ށi�k�����j
�@�@�@�@�U�O�m���|�Q�R�e���|�P�T�b���ł͂P�P�T�O���܂Ŏg�p�ł��A�퉷�ł̒�R�͂P�D�P�P�ʃ����B
�@�@�e���|�m���|�b���{�r���A��y�ށi�k�����j
�@�@�@�@�S�R�e���|�R�T�m���|�Q�O�b���łP�P�O�O���A��R�͂P�D�O�T�ʃ����B
�@�@�@�@�S�W�e���|�R�O�m���|�Q�O�b���łP�O�T�O���A��R�͂P�D�O�R�ʃ����B
�@�@�@�@�T�S�e���|�Q�O�m���|�Q�S�b���łP�O�T�O���A��R�͂O�D�X�T�ʃ����B
�@
�E�J���^��Kanthal�i�S�b���n�j
�@�e���|�P�Q�`�R�O�b���|�S�`�V�`�������ōō��P�S�O�O���܂Ŏg�p�ł���B
�@�`����������ɏ]���čō��g�p���x���㏸���A��R�������Ȃ�B
�@�t�F���C�g���B
�@�@�Q�O�b���|�U�`���łP�S�O�O���A��R�͂P�D�S�T�ʃ����B
�@�@�Q�Q�b���|�T�`���łP�R�O�O���A��R�͂P�D�R�X�ʃ����B
�@�@�Q�O�b���|�S�`���łP�P�O�O���A��R�͂P�D�Q�R�ʃ����B
��R����
�@�@��R�����Ƃ��Ă͂m���|�b���A�m���|�e���A�b���|�m���A�b���|�l���������g�p����A���ɐ�����R�A��R�c�v�ɂ͂b���|�m���A�b���|�l���������g�p����A
�@��R�̉��x�W�������������Ƃ����߂���B
�@�@�b���|�m���n�����͒ቷ���M�i�����h�~�A�֍����j�ɂ��g�p�����B
�@�@���̑��p�r�ɂ͔M�d������B
�E�b���|�Q�`�S�T�m���n�@�@Radio alloys�i�b���|�Q�`�Q�Q�m���j�ACuprothal�i�T���h���B�b�N�Ёj
�@�@�b���|�S�S�D�O�m���|�P�D�O�l���|�O�D�T�e���@�@�U�O�O���A�O�D�S�X�ʃ����A���x�W���Q�O������
�@�@�b���|�Q�R�m���|�P�D�T�l���@�@�@�@�@�@�@�@�@�@�S�O�O���A�O�D�R�O�ʃ����A�P�W�O������
�@�@�b���|�P�P�m���@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�S�T�O���A�O�D�P�T�ʃ����A�S�T�O������
�@�@�b���|�U�m���@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�R�O�O���A�O�D�P�O�ʃ����A�V�O�O������
�@�@�b���|�Q�m���@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�R�O�O���A�O�D�O�T�ʃ����A�P�S�O�O������
�@

�@
�E�R���X�^���^���ށ@�@�b���|�m���i�{�l���A�e���j
�@�@�T�V�b���|�S�R�m���@�@�@�O�D�T�O�ʃ����A�}�Q�O
�@�@�T�T�b���|�S�T�m���@�@�@�O�D�T�O�ʃ����A�}�S�O
�@�@�T�R�b���|�S�S�m���|�R�l���@�@�O�D�T�Q�ʃ����A�}�V�O
�@�@�T�T�b���|�S�T�m����T�^�Ƃ��A�l���A�e����Y���������̂�Constantan�AAdvance�AEureka�AFerry�ȂǂƌĂ��B
�@�@���l��Monel�A���Z���@�@�R�O�b���|�U�V�m���|�Q�e���|�P�l���i�{�r���j�@�@�@�O�D�T�O�ʃ����A�P�S�T�O������
�@�@Isazin�@�b���|�Q�R�m���|�P�D�T�l���@�P�W�O�������@�O�D�R�O�ʃ���
�@�@Isotan�@�b���|�S�S�m���|�P�l���@�U�O�O���A�|�W�O�`�{�S�O�������A�O�D�S�X�ʃ����A
�@�@Copel�R�[�y���@�@�@�T�S�b���|�S�T�m���|�O�D�R�e���@�@�@�@�O�D�S�V�ʃ����A�}�Q�O
�@�@�m���͂T�O�`�V�O�b���|�P�T�`�R�T�y���|�T�`�R�T�m���̍����A�m���������قǃo�l���ɂ�����A�y���������قǍ����x�B
�@�@�@�U�S�b���|�P�W�m���|�P�W�y���@�@�@�U�D�O�h�`�b�r
�@�@�@�U�Q�b���|�P�S�m���|�Q�S�y���@�@�@�U�D�X�h�`�b�r
�@�@�@�T�U�b���|�P�W�m���|�Q�U�y���@�@�@�T�D�U�h�`�b�r
�@�@�v���`�m�C�hPlatinoide�@�@�T�S�b���|�Q�T�m���|�Q�O�y���@�@�@�O�D�R�S�ʃ���
�@�@�j�b�P����Nickelin�@�@�@�@�T�S�b���|�Q�U�m���|�Q�O�y���@�@�@�O�D�S�R�ʃ���
�E�b���|�l���n
�@�@�}���K�j��Manganin�@�@�@�b���|�P�O�`�P�R�l���|�P�`�S�m���A��\�I�Ȃ��̂͂b���|�P�Q�l���|�Q�m���A�O�D�S�S�ʃ����A�Q�O�������B
�@�@Ohmal �@�@�@�@�@�@�@�b���|�X�`�P�P�l���|�R�D�U�m���|�O�D�R�e���|�O�D�P�r��
�@�m���̑���ɂr���A�f���A�r��
�@�@Zeranin�@�@�b���|�V�l���|�Q�D�R�r���@ �@�@�@�@�@�@�O�D�Q�X�ʃ����A�}�P�O�������@�@�@�@
�@�@�b���|�X�C�T�l���|�O�D�V�f���@�@�@�@�@�@�O�D�R�V�ʃ���
�@�b���|�l���|�`���n
�@�@Isabellin�@�@�@�@�@�@ �b���|�P�R�l���|�R�`���@�@�@�@�@�O�D�T�O�ʃ����@�@
�@�@Therlo�@�@�@�@�@�@ �@�b���|�X�D�T�l���|�T�D�T�`���@�@�@
�@�@Novokonstant�@ �@�b���|�P�Q�l���|�S�`���|�P�D�T�e���@�@�O�D�S�T�ʃ���
�E�m���|�e���n�@Nifethal�i�T���h���B�b�N�Ёj
�@�@�V�Q�m���|�e���@�T�O�O���܂ŁA�O�D�Q�ʃ����B
�@�@�T�Q�m���|�e���@�U�O�O���܂ŁA�O�D�R�V�ʃ����B
�@�@�S�Q�m���|�e���@�U�O�O���܂ŁA�O�D�U�R�ʃ����B
�@�@Resistherm�iIsabellenhutte�j�@�@�m���|�R�O�e���|�O�D�U�`���|�O�D�T�l���|�O�D�R�b���@�@�U�O�O���܂ŁA�O�D�R�R�����A�R�Q�O�O������
�E�m���|�b���|�`���n
�@�@�R�T�`�X�T�m���|�b���|�`���i�{�b���A�e���A�l���j
�@�@Karma�@�@�@�@�m���|�Q�O�b���|�R�`���|�R�e���@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�P�D�R�R�����A�}�T������
�@�@Evanohm�@�@ �m���|�Q�O�b���|�Q�D�T�`���|�P�D�V�b�� �@�@�@�@�@�@�@�@�@�@�@�@�P�D�R�R�����A�Q�O������
�@�@Isaohm�@�@�@ �m���|�Q�O�b���|�R�D�T�`���|�P�r���|�O�D�T�l���|�O�D�T�e���@�@�P�D�R�Q�����A�}�T�O������
�@�@�`���|�l���|�r���n
�@�@�@�@�`���|�P�R�l���|�X�r���@�@�O�D�T�V�ʃ���
�@�@�`�������n
�@�@�@�@�`���|�b���A�b��
�@�@�@�@�`���|�Q�b���@�O�D�R�R�ʃ���
�E��R�c�v�p����
�@�@Constantan�AManganin�AIsoelastic�AKarma�Ȃǂ����p�����B
�E�M�d�Ηp����
�@�@�N�������@�@�@�X�O�m���|�P�O�b��
�@�@�@���W�O�m���|�Q�O�b���iChromel A Nichrome 80-20�j�A�U�O�m���|�P�U�b���|�Q�S�e���i Chromel C Nichrome60�j
�@�@�A�������@�@�@�X�S�m���|�R�`���|�P�r���|�Q�l��
�i�P�S�|�S�j�`�������Ƃb������
�i�P�S�|�S�|�P�j�A���~�j�E������
�@�`���͑����̋����Ƌ����ԉ��������`������B
�@�a���A�r���A�y���A�f���C�f�����Ƃ͉��������`���������������^�ƂȂ�B
�@�`���ւ̌ŗn�ʂ������̂͂y���A�`���A�l���A�k���A�f���A�b���A�f���A�r���ȂǁB�i�ŗn���P�������ȏ�j
�@�`�������ł͌ŗn�d���͊��҂ł����A�����d�������H�d�������p�����B
�@�`�������ł͂`���|�b���A�`���|�l���A�`���|�y���A�`���|�`���ȂǂŎ����d���̉ߒ��ɕꑊ�Ɛ������̗ǂ�
�f�o�]�[�����`�������B
�@

�@�@�@�@�@�@�@�T�^�I�`���n�Q����Ԑ}

�@�@�@�@�@�@�@�`���ւ̎�X�Ȍ��f�̌ŗn��
�@�W�L�p����
�@�@�P�w�w�w�@�@�X�X�D�O�O���ȏ㏃�`���A��v�s�����͂r���A�e���B
�@�@�Q�w�w�w�@�@�`���|�`�U�b���n
�@�@�@�Q�O�P�S
�@�@�@�Q�O�P�V�F�W�������~���A�`���|�S�b���|�O�D�T�l���|�O�D�T�l��
�@�@�@�Q�O�Q�S�F���W�������~���A�`���|�S�D�S�b���|�P�D�T�l���|�O�D�U�l��
�@�@�@�Q�O�P�P�F���퍇���A�o���A�a���Y���B
�@�@�R�w�w�w�@�`���|�l���n
�@�@�@�R�O�O�S�A�R�P�O�S�@�l���Y���B
�@�@�S�w�w�w�@�`���|�r���n
�@�@�@�X�ɂb���A�m���A�l�����ʂőϔM������B
�@�@�T�w�w�w�@�`���|�l���n�B
�@�@�U�w�w�w�@�`���|�l���|�r���n�B
�@�@�V�w�w�w�@�`���|�y���|�l���B
�@�@�@�b���̗L���B
�@�@�@�V�O�V�T�@���X�W�������~���A�`���|�T�D�U�y���|�Q�D�T�l���|�P�D�U�b��
�@�@��M�����^�A���H�d���^
�@�@�@�@�`���|�l���n�A�`���|�l���n�A�`���|�r���n�B
�@�@�M�����^�A�����d���^�@
�@�@�@�@�`���|�b���n�i�b���`���Q�j�A�`���|�b���|�l���n�A�`���|�l���|�r���n�i�l���Q�r���͏o�j�A�`���|�y���|�l���n�i�l���y���Q�͏o�j�A�`���|�y���|�l���|�b���n
�@���`���|�b���|�k���n�i�`���R�k���͏o�j
�@�@�@�Q�`�R�b���|�P�D�S�`�Q�D�O�k���i�{�y���A�l���A�l���A�y���j�A�y�ʉ��A�y���ňٕ������P�A
�@�@�@�Q�O�X�O�F�`���|�Q�D�P�b���|�Q�D�O�k���|�O�D�P�O�y��
�@�@�@�W�O�X�O�F�`���|�Q�D�S�T�k���|�P�D�R�b���|�O�D�X�T�l���|�O�D�P�Q�y��
�@

�@�@�@�@�@�`���|�b���n��Ԑ}

�@�@�@�@�`���|�l���n��Ԑ}

�@�@�@�@�`���|�r���n��Ԑ}

�@�@�@�`���|�l���n��Ԑ}

�@�@�@�`���|�y���n��Ԑ}

�@�@�@�`���|�k���n��Ԑ}
�i�P�S�|�S�|�Q�j�b������
�@�b���̍������f�ŋ����ԉ��������`�����Ȃ��̂�
�@�@�m���A�`���A�b���A�e���A�b���A�o���A�l���A�m���A�a������
�@�����ԉ��������`��������̂�
�@�@�y���A�`���A�r���A�o�A�a���A�l���A�s���A�y���A�r���A�r���A�b���A�h�����ł���B
�`�j�@�b�������̋������@
�@�b�������̋������@�ɂ͌ŗn�����A�͏o�����A�X�s�m�[�_������������B
�@�b���|�a���A�b���|�b�������͂f�o�]�[�����`������Ƃ����B
�@�b�������ł� �b���|�s���A�b���|�m���|�r���A�b���|�m���|�r���A�b���|�b���|�r���A�b���|�a���A�b���|�r���A�b���|�h���A�b���|�`���A�b���|�r���A
�b���|�r���A�b���|�l���A�b���|�b���Ȃǂ����E�����^�i�s�A���^�j�̐͏o������B
�@�E�ŗn�����^
�@�@�@�@�@�@�y���A�m���A�`���A�r���A�l���A�l���A�h���A�i�r���j�ȂǁB
�@�@�@�@�@�@�b���|�r���n�͏�Ԑ}��͏퉷�ł̓��{�Â̂Q���ł��邪�A���̔����͋N����ɂ����A��X���r���܂ł̓�����
�@�@�@�@�@�������ƃ����͏o����Ƃ����B
�@�@���j�����^�i�b���|�y���n�j
�@�@�@�@�����ԉ��������`�����A�g���ɂ�胿�A���{���A���E�E�E�Ƃ����g�D���Ƃ�B
����������
�@�@�@�@�����ł͂y���͂b����蕅�H�A�n�o���₷���A���̉��P�₻�̑������̉��P�̂��ߑ�R������Y�����邪�A���̏ꍇ
�@�@�@�̑g�D�ւ̉e����Guillet�͈������ʂŎ������B
�@�@�@�@�y�����ʁ��y��%+10.0�r��%+6.0�`��%+2.0�r��%+2.0�l��%+1.0�o��%+1.0�b��%+0.9�e��%+0.5�l��%-1.3�m�� (wt%)
�@�@�@�@�@�b���|�y���n��Ԑ}
�@�@�@

�@�@�@�@�@�@�@�b���|�l���n
�@�@�@�@

�@�@���j�b���|�r���^�i���́j
�@�@�@�@

�@�@�@�@�@�@�b���|�`���n
�@�@�@�@

�@�@�@�@�@�@�b���|�r���n
�@�@

�@�@���j�b���|�l���n
�@�@�@�@�@�@�����ԉ��������`�����Ȃ��B
�@�@�@

�@
�@�@���j�b���|�m���i�S���ŗn�^�j
�@�@�@�@�@

�@�E�͏o����
�@�@���j�ŗn�x�ω��^
�@�@�@�@�@�`���A�b���A�e���A�b���Ȃǂ͂b���Ɖ��������`�����Ȃ��A�o���A�a���͉���ނɗ��p�����B
�@�@�@�@�@�@�@�b���|�`���n
�@�@�@�@�@

�@�@�@�@�@�@�@�@�@�b���|�b���n
�@�@�@

�@�@�@�@�@�@�@�@�@�b���|�e���n�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�b���|�b���n
�@�@�@�@

���t�s�n��xretrograde solubility
�@�ʏ�A�n���̗n��x�͉��x�~���ɔ����n��x���������邪�A�b���|�e���n�A�b���|�b���n�ł͉��x�~���ɔ���
�n��x����������t�s�n��xretrograde solubility�������B
�@�@

�@�@�@�@�@�@�����ԉ������`���^
�@�@�@�@

�@�@�@

�@�@�@�@

�@�@���j�R���n�ł̓Y���������m�̐͏o�d��
�@�@�o�A�r�����͂b����艻�������`�����₷�����f�Ɣ������ĉ������Ƃ��Đ͏o�B
�@�@�r���ł͂b���|�m���|�r���i�R���\�������j�A�b���|�b���|�r���A�b���|�b���|�r���Ȃǂm���A�b�����悭���p�����B
�@�@���̂ق��e���A�b���X�ɂl���A�l���Ȃǂ��P�C�������`������B
�@�@�o�ł͂b���|�o�A�m���|�o�A�e���|�o�A�b���|�o���悭���p����A�l���A�l���A�b���A�s���A�y�����������������`���B�@�@
�@�@�a�����m���A�b���A�e�����ƃx�����E���������`������Ƃ����B
�@�@���邢�͂y���A�s�����Ƃ̉������i�b���|�y���A�y���[�s���A�s���[�b���A�e���|�s���E�E�E�j���͏o����B
�@�E�X�s�m�[�_������
�@�@�@�@�b���|�s���n�A�b���|�m���|�r���n�A�b���|�m���|�b���n�ȂǁB
�@�@�@�@

�@�@�@�@

�@�E�K���i�q�`��
�@�@�@�@�b���|�`���n
�@�@�@�@�@

�@�@�@�@�b���|�o��
�@�@

�@�@�@
�a�j�@�����̑��ϑ�
�@�@�b�������̃����ɂ̓}�b�V�u�ϑԁA�x�C�i�C�g�ϑԁA�K�����A�}���e���T�C�g�ϑԂȂǂ�������̂��m���Ă���B
�@�a�|�P�j�}�b�V�u�ϑ�
�@�@�@�b���|�f���A�b���|�y���ł͍��������i�������A�s�K�����j�͋}��Ń��������̃}�b�V�u�ϑԂ��s���B
�@�@�@�b���|�f���ł̓����̂ق��Ƀ����Ă��̃}�b�V�u�ϑԕϑԂ��N����A�L���͈͂Ń����ƃĂ��̂Q����Ԃ�������B
�@�@
 �@
�@
�@�@�@�@�@�@�@�@�b���|�y�������}�b�V�u�ϑԈ�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�b���|�f�������̃}�b�V�u�ϑԈ�
�@�a�|�Q�j�x�C�i�C�g�ϑ�
�@�@�@�b���|�y���ł̓����̋}��Ő�������������P���i�a�Q�\���j�͂Q�O�O���̍P�����M�Ńx�C�i�C�g�ϑԂ�����B
�@�@�@�b���|�`���n���x�C�i�C�g�ϑԂ��s���B
�@�a�|�R�j�K�����ƃ}���e���T�C�g�ϑ�
�@�@�@�b���|�`���A�b���|�r���A�b���|�y���A�b���|�f���̃����̓x���g���C�h�^�̃q���[���E���U���[�d�q�������ie/a���R�^�Q�j��
�@�����ԉ������ŁA�������͕s�K���^�̂`�Q�^�i�������j�ł���A�K���^���P�i�a�Q�A�c�n�R�A�k�Q�P���j���ւă}���e���T�C�g���L�ϑ�
�@���邱�Ƃ��m���Ă���B
�b�j�b�������̎��
�@�������͓��d���ƔM�`�����ɗD��A�����́A�h�b�Ȃǂ̃p�b�P�[�W�p���[�h�E�t���[����R�l�N�^�[�A���M�Ȃǂ�
�d�C�E�d�q�ޗ��̒��S�ƂȂ��Ă���B
�@���̓��d���͍����x�Ȃ��̂قǍ����A������̋��x�͍����ʂ������قNj����B
�@�]���ē��d���Ƌ��x�̊W�͑������Ă���B
�@���h�`�b�r�F�Q�O���łP�D�V�Q�S�P�ʃ��E�����̍��ەW�������Ƃ���B
�@

�@�@�@�@�@�@�@�@�@�@�@�@�����ʂƓ��d��
�@

�@

�@�������̋�����
�@�@�ŗn�����E�E�E�r���A�y���A�m���A�l���A�l���A�r���ȂǁB
�@�@�͏o�����E�E�E�ȉ��̂悤�ȕ��@
�@�@�@�b���A�y���A�`���A�b���A�e���A�a���A
�@�@�@�b���|�o�A�e���|�o�A�m���|�o�A�b���|�o������
�@�@�@�m���[�r���A�b���[�r���A�b���[�r��������
�@�@�@�b���|�y��������
�@�@�X�s�m�[�_�������E�E�E�b���|�s���A�b���|�m���|�r���A�b���|�m���|�b���ȂǁB
�@�@���U�����E�E�E�ȉ��̂悤�ȕ��@
�@�@�@�`���Q�n�R
�@�@�@�m���F�}��ÌŁA���J�j�J���E�A���C���O�l�`�@�Ȃǂő��ʂ̕��U�i�P�O���m�����j
�@�@�@�@�@�b���C�v�A�s���A�m���A�l���A�u�Ȃǂ��\��������Ƃ����B
�Ȃǂ����p�����B
�@
�@�ȉ��b�c�`�i�č��̓��J������j�o�^�m���D�ɉ����ďЉ��B
�@�E�b�P�w�w�w�w
�@�@�@���b���Ɩ�X�X�D�R���b���܂ł̍��b�������Ɩ�X�U���b���܂ł̑��ɋK�肳��Ȃ��b���������܂ށB
�@�@�@���S�ƂȂ鍇���͋�����i�b���|�`���j�A�������i�b���|�r���j�A�S�����i�b���|�e���j�A�W���R�j�E�����i�b���|�y���j�A
�@�@�N�������i�b���|�b���j�A�R�o���g���i�b���|�b���j�A�j�b�P�����i�b���|�m���j�A�}�O�l�V�E�����i�b���|�l���j�A
�@�@�x�����E�����i�b���|�a���j�A�`�^�����i�b���|�s���j�Ȃǂł���B
�@�@�@�d�q�ޗ��Ƃ��ďd�v�Ȃ��̂������B
�@�@��������
�@�@�@�@�d�i�d�C���j�@�@�@�@�X�X�D�X�U���ȏ�@�s�����͂r���A�r���A�o���A�e���A�Ȃǂœ��ɂa���͂O�D�O�O�P���ȉ��ƌ������B�@�@
�@�@�@�@���_�f���n�e�b�@�@�@�@�@ �X�X�D�X�T���ȏ�A�^��n���łn�F�O�D�O�O�P���ȉ��B
�@�@�@�@�^�t�s�b�`���s�o�b�@�@�@�@�X�X�D�X�O���ȏ�A�d�C�����琸�B�A�n�F�O�D�O�Q�|�O�D�O�T���B
�@�@�@�@�����E�_���c�g�o�@�@�@�@ �X�X�D�X�O���ȏ�A�o�F�O�D�O�S���ȉ��B�@
�@�@�@�@�����_�f���̉��nj^
�@�@�@�@�@�@�@������_�f���n�e�r�@ �@�O�D�P���ȉ��`���B
�@�@�@�@�@�@�@���̂ق� �y�����薳�_�f���A�r�������_�f���ȂǁB
�@�@�@�����悻�X�X�D�U���b���̓������̑�\�I�Ȃ��̂�
�@�@�@�@�@�b���|�`���@
�@�@�@�@�@�b���|�e���|�o
�@�@�@�@�@�b���|�r���i�{�o�j
�@�@�@�@�@�b���|�y��
�@�@�@�@�@�b���|�b���|�o
�@�@�@�����悻�X�X�D�R���b���̓������̑�\�I�Ȃ��̂�
�@�@�@�@�@�b���|�`��
�@�@�@�@�@�b���|�`���|�n�i�`���Q�n�R�j
�@�@�@�@�@�b���|�e���|�o�{�m���A�r���A�y���A�l��
�@�@�@�@�@�b���|�r���|�o�{�e���A�m���A�y��
�@�@�@�@�@�b���|�b���{�y���A�r���A�y���A�r��
�@�@�@��X�U���b���̓������̑�\�I�Ȃ��̂�
�@�@�@�@�@�b���|�e���|�o�{�m���A�r���A�y���A�l��
�@�@�@�@�@�b���|�r���|�o�{�e���A�m���A�y���@�@�@�@�i���ǃ������j�@�@
�@�@�@�@�@�b���|�m���|�o�{�y��
�@�@�@�@�@�b���|�b���{�y���A�r���A�y���A�r���A�s��
�@�@�@�@�@�x�����E�����i�b���|�a���{�b���A�m���j
�@�@�@�@�@�`�^�����i�b���|�s���j
�@�@�@�@�@�}�O�l�V�E�����i�b���|�l���|�o�j
�@�@�@�@�@��R���\�������i�b���|�m���|�r���{�y���A�r���A�l���A�b���j�@�@���S�͂b�U�w�w�w�w
�@�@�@�@���̂ق�
�@�@�@�@�@�b���|�y���i�{�e���A�o�A�l���j�A�b���|�r���|�m���i�{�o�j�A�j�b�P�����F�b���|�m���[�r���i�{�e���A�o�A�y���A�l���j�A
�@�@�@�@�b���|�r���|�y���i�{�e���A�o�A�l���A�r���j�ȂǁB
�@�E�b�Q�w�w�w�w
�@�@�@�b���|�y���i�����j�n
�@�@�@�@����Gilding�@�@�@�@�@�@�@�X�T�|�T�y��
�@�@�@�@���Ɛ�bronze�@�@�@�@�X�O�|�P�O�y��
�@�@�@�@��ΐ��@�@�@�@�@�@�@�@�W�V�|�P�R�y��
�@�@�@�@�ԉ���brass�@�@�@�@�@�@�W�T�|�P�T�y��
�@�@�@�@�ቩ���@�@�@�@�@�@�@�@�@ �W�O�|�Q�O�y��
�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�V�T�|�Q�T�y��
�@�@�@�@�J�[�g���b�W�����i�V�|�R�����j�@
�@�@�@�@�������@yellow brass�@�@�@�U�T�|�R�T�y��
�@�@�@�@Muntz Metal�i�U�|�S�����j�@�@�@�@
�@�@�@���O���@�@�@�@�y�����Q�O
�@�@�@�����Ǘp���@�@�X�W�D�O�`�X�X�D�O�b���|�y���@�@�@�@
�@�@�@���T�~�d�݁@�U�T�b���|�R�T�y��
�@�@�@
�@�E�b�R�w�w�w
�@�@�@�b���|�y���|�o���i���퉩���j�n
�@�@�@�T�T���b�����U�S�A�O�D�P���o�����S�D�T�A�y�����S�T
�@�E�b�S�w�w�w�w�@�@
�@�@�@�b���|�y���|�r���i�r���������j�n
�@�@�@�O�D�P���r�����T�D�T�A�y�����S�T
�@�@�@�@�A�h�~�����e�B�����G�V�|�R�����x�[�X�ɂP���r���@�@
�@�@�@�@�l�[�o�������F�U�|�S�����x�[�X�ɂP���r���@�@
�@�@�@�@�r�X�}�X���퉩���F�U�|�S�x�[�X�ɂa�����R�D�O�@�@
�@�@�@���P�O�~�d�݁F�b���|�R�D�T�y���|�P�D�T�r��
�@�E�b�T�w�w�w�w
�@�@�@�b���|�r���|�o�i�������j�n�@�@�@�@�@
�@�@�@�R���r�����P�O�A�O�D�O�R���o���O�D�R�T�A�{�m���A�y���A�e��
�@�E�b�U�w�w�w�w�@�@
�@�@�@��������Ȃ킿�b���|�`���A�l�����A�r���A�m���n
�@�@�@���͉������Ȃ킿�����ɂl���A�`���A�e���A�r���A�m���A�r���Ȃǂ�Y����������
�@�@�@�R���\���������Ȃ킿�b���|�m���|�r���n�łm���|�r���̐͏o�d���𗘗p��������
�@�@�Ȃǂ��܂܂��B
�@�@�@�@�A���~��
�@�@�@�@�@�b���|�`���{�e���A�m���A�l���A�r��
�@�@�@�@�@�@�b���|�`���|�e���@�@
�@�@�@�@�@�@�b���|�`���|�m���i�A���~�j�b�P�����j�@�@
�@�@�@�@�@�@�b���|�`���|�r���@�@
�@�@�@�@�}���K����
�@�@�@�@�@�b���|�l���|�`���{�e���A�m���@
�@�@�@�@�V���R�����@
�@�@�@�@�@�r���{�l���A�y���A�e���A�r���@
�@�@�@�@�@�O�D�U���r�����S�D�O
�@�@�@�@�R���\������
�@�@�@�@�@�b���|�m���|�r���{�y���A�r���A�l���A�l���A�b����
�@�@�@�@�@�O�D�S���m�����S�A�O�D�O�T���r�����P�D�Q
�@�@�@�@���͉����@�@
�@�@�@�@�@�b���|�y���i�����j���x�[�X�ɂl���A�`���A�e�����P�`�R�����x�A�X�ɂm���A�r���A�r������Y��
�@�@�@�@�@�@�b���|�y���|�e��
�@�@�@�@�@�@�b���|�y���|�l���@
�@�@�@�@�@�@�b���|�y���|�r��
�@�@�@�@�@�@�b���|�y���|�`���i�A���~�����j
�@�@�@���y��ٗp�����@�U�O�b���|�y���|�P�r���|�O�D�T�o���|�O�D�T�l���@
�@�E�b�V�w�w�w�w
�@�@�@�b���|�m���i�����A�L���v���E�j�b�P���j�n�Ƃb���|�m���|�y���i�m���A�m��j�n����Ȃ�X�s�m�[�_���������܂܂��B
�@�@�@�@�b���|�m���i�����A�L���v���E�j�b�P���j�n�@�@
�@�@�@�@�@�b���|�m���{�r���A�e���A�y���A�l��
�@�@�@�@�@�T�m���A�V�m���A�P�O�m���A�Q�O�m���A�R�O�m���A�i�S�T�m���j�@�@�@
�@�@�@�@�b���|�m���|�y���A�b���|�y���|�m���i�m���A�m��j�n�@
�@�@�@�@�@�X�O�`�S�O�b��
�@�@�@���j�b�P������
�@�@�@�@�@�T�O�O�~�ݕ��͂b���|�Q�O�y���|�W�m���Ńj�b�P�������Ə̂���B
�@�@�@�@�R���\������
�@�@�@�@�X�s�m�[�_������
�@�@�@�@�@�b���|�X�m���|�U�r���@
�@�@�@�@�@�b���|�Q�P�m���|�T�r��
�@�@�@�@�@�b���|�R�O�m���|�R�b��
�@�@�b�W�w�w�w�w
�@�@�@��������
�@�@�@�@���b��
�@�@�@�@�b���|�a���{�i�b���A�r���A�m���j
�@�@�@�@����
�@�@�@�@�@�b���|�y���{�r���A�o���A�m���A�l���A�e��
�@�@�@�@�V���R���i�V���W���j��
�@�@�@�@�@�b���|�y���|�r���{�r��
�@�@�@�@���͉���
�@�@�@�@ �r�X�}�X��
�@�@�@�@�@�b���|�y���|�r���[�a��
�@�@�b�X�w�w�w�@�@
�@�@�@������
�@�@�@�@�r����
�@�@�@�@�@�b���|�r���A�V�`�P�X�r��
�@�@�@�@�@�{�y���A�o���A�l���A�e�����m���A
�@�@�@�@�������@�@
�@�@�@�@�@�b���|�r���|�o
�@�@�@�@�@�O�D�O�T���o���P�D�O
�@�@�@�@�����@
�@�@�@�@�@�b���|�o���|�r���{�m���A�y���A�o
�@�@�@�@�@����@
�@�@�@�@�A���~��
�@�@�@�@�}���K����
�@�@�@�@�j�b�P����
�@�@�@�@
�@�@�@�@���̑�
�@�@�@�@�@�C���F�b���|�P�O�r���|�Q�y��
�@�@�@�@�@bell bronze�F�b���|�Q�O�r��
�@�@�@�@�@malleable bronze�F�b���|�W�r��
�@�@�@�@
�c�j�d�q�ޗ��p
�c�|�P�j���[�h�E�t���[��

�@�@�@�@�@�@�h�b�p�b�P�[�W�̖͎��f�ʐ}�ƊO��
�@
�@�@�����́A�h�b�̃p�b�P�[�W�̃��[�h�t���[���ɗ��p�����̂͂e���|�S�Q�m���i�S�Q�A���C�j��
�@�b�������ł���B
�@�@�S�Q�A���C�͎����Ƃ̖������ɂ�����邪���d���A�`�M���͓�������������Ă���̂�
�@���݂͓��������嗬�Ƃ����B
�@�@�g�p����铺�����͓S�����i�b���|�O�D�P�e���|�O�D�O�R�o�A�b���|�Q�D�R�e���|�O�D�P�Q�y���|�O�D�O�R�o�Ȃǁj�A
�@�������i�b���|�O�D�P�T�r���|�O�D�O�P�o�j�A�N�������i�b���|�O�D�R�b���|�O�D�Q�T�r���|�O�D�Q�y���j�A�W���R�j�E�����i�b���|�O�D�O�Q�y���A�b���|�O�D�P�y���j�Ȃǂ�
����������R���\�������i�b���|�R�D�Q�m���|�O�D�V�r���|�P�D�Q�T�r���|�O�D�R�y���j�Ȃǂ��g�p�����B
�c�|�Q�j���M�ޗ�
�@�@�q�[�g�E�V���N�A�q�[�g�E�X�v���b�_�[�i���M�j�A�a�f�`�̃X�e�B�t�i�[�i�⋭�j���ɔM�`�����̂悢���������g�p�����B
�@�@


�@�@�@�@�X�e�B�t�i�[�@�@�@�@�@�@�@�@�@�@�@
�@

�c�|�R�j�R�l�N�^�[
�@�@�R�l�N�^�[�ɂ͋��x�̑傫���x�����E�����A�R���\�������A�������A�X�s�m�[�_�������Ȃǂ���ɗ��p�����B
���o�l�ޗ�
�@�@�������ł̓o�l�ޗ��Ƃ��Ă͂����A�m���A�x�����E�����A�`�^�����A�b���|�m���|�r���Ȃǂ����p�����B
�i�P�S�|�T�j�@���Z�_����
�@�S�C�T�C�U�����u�̌ŗn��������ŁA�Y�����̐͏o�d����_�������U���������p����Ă���B
�@���H�͕�������i�Č��j�Ɛ^��n������ł���B
�@�p�r�͌��q�͂ƉF���ł���B
�i�P�S�|�T�|�P�j�@�v����
�@�@���@����B
�@�E�w�r�[�E���^��
�@�@�@�v�ɂQ�`�P�O���̂m���E�e���܂��͂m���E�b���B�@�@
�@�@�@�t���Č��A�Č������B�p�r�͐��i���������d���j��
�@�E�v�|�i�P�O�`�T�O�j�b���F�d�C�ړ_�A���d���H�E�X�|�b�g�n�ړd�ɁA���M�i�P�O�`�R�O�b���j��
�@�E�v�|�i�Q�O�`�V�O�j�`���F�d�C�ړ_
�@�@�@
�@�����d����
�@�@�@���d�����Ƃ͂v�b�i�Y���^���O�X�e���j���b���ȂǂŏČ��������̂ł���B
�@�@�@�����ނƂ��Ă͂b���̂ق��m���A�b���Ȃǂ�����A�s���b�A�s���b�Ȃǂ�Y���������̂�����B
�@�@�@��ʓI�ɂ͊e��Y�����s���b�A�b���b�A�������s���m�A�퉻���s���a�Q�C�l���a�A�v�a�����m���A�b���Ȃǂ�
�@�@�����A�Č������ޗ����T�[���b�gcermet�i�Z���~�b�N�Ƌ����̕����ޗ��j�Ə̂���B
�@�@�@�������퉻���͋��L�������������k���ȏČ��̂삵�ɂ����B
�@�E���U����
�@�@�@�P�`�Q�k���Q�n�R�@�@
�@�@�@�Q�D�O�b���n�Q�@�@
�@�@�@�Q�D�T�k���Q�n�R�{�O�D�O�V�y���n�Q
�@�@�@�P�`�Q�s���n�Q
�@�E�v�|�i�T�܂��͂Q�U�j�q���i�{�g���A�b�j
�@�@
�i�P�S�|�T�|�Q�j�@�s������
�@�@�s���|�Q�D�T�v�@�i�q�O�T�Q�T�Q�j
�@�@�s���|�V�D�T�v
�@�@�s���|�P�O�v�@�i�q�O�T�Q�T�T�j
�@�@�s���|�W�v�|�Q�g���@�i�s�|�P�P�P�j�@
�@�@�s���|�P�O�v�|�Q�D�T�g���|�O�D�O�P�b�@�i�s�|�Q�Q�Q�j�@�@
�@�@�s���|�W�v�|�P�q�d�|�O�D�V�g���i�|�O�D�O�Q�T�b�j�@�`�r�s�`�q�|�W�P�P�i�b�j
�@�@�s���|�R�O�m��
�@�@�s���|�S�O�m���@�i�q�O�T�Q�S�O�j
�@�@���`�r�s�l�@�a�V�O�W�K�i
�@�@�@�q�O�T�Q�T�Q�A�q�O�T�Q�T�T�A�q�O�T�Q�S�O
�i�P�S�|�T�|�R�j�@�l������
�@�E�ŗn����
�@�@�@�l���|�Q�O�`�T�O�v
�@�@�@�l���|�S�܂��͂S�O�q��
�@�@�@�l���|�P�P�s��
�@�E�Y�����`��
�@�@�@�s�y�l�@�@�l���|�O�D�T�s���|�O�D�O�W�y���|�O�D�O�R�b
�@�@�@�l�g�b�@�@�l���|�P�D�Q�g���|�O�D�P�b
�@�E���U����
�@�@�@�O�D�R�`�O�D�V�܂��͂O�D�O�R�k���Q�n�R�@
�@�@�@�O�D�T�x�Q�n�R�i�{�O�D�O�W�b���n�Q�j
�@�@�@�P�D�V�y���n�Q�@
�@�E�l���|�b���@
�@�@�@�P�T�`�R�O�b��
�i�P�S�|�T�|�S�j�@�m������
�@�@�@�m���|�P�y���@�i�m���P�y���j
�@�@�@�m���|�P�y���|�O�D�P�b�@�i�o�v�b�|�P�P�j
�@�@�@�m���|�P�O�g���|�P�s���@�i�b�P�O�R�j
�@�@�@�m���|�P�O�v�|�Q�W�s���|�P�y���@�i�e�r�W�T�j
�@�@�@�m���|�P�O�v�|�P�O�g���|�O�D�Q�x�@�i�b���P�Q�X�x�j
�@�@�@�m���|�P�O�v�|�Q�D�T�y�@���i�b���V�Q�T�j
�@�@�@�m���|�R�O�g���|�X�܂��͂P�T�v
�@�@�@�m���|�P�O�v�|�P�O�s���@�i�r�b���Q�X�P�j
�i�P�S�|�T�|�T�j�@�y������
�@�@���q�F�p�ɂ͂r����Y���������̂Ƃm����Y���������̂�����B
�@�@�@Zircaloy�|�Q�@�y���|�P�D�T�r���|�O�D�P�T�e���|�O�D�P�b���|�O�D�O�T�m���@�i�g�b�o�j
�@�@�@Zircaloy�|�S�@�y���|�P�D�T�r���|�O�D�Q�e���|�O�D�P�b���@�i�g�b�o�j
�@�@�@�y���|�m���@�@�y���|�Q�D�T�m���i�{�O�D�Q�e���j�@�i�g�b�o�{�a�b�b�j
�@�@�q�F�̏��ƃO���[�h�̂��Ƃł́@�g����Y���������̂�����B
�@�@�V�O�Q�@�@�g�����S�D�T�A�e���{�b�����O�D�Q�A�b���O�D�O�T�@�i�g�b�o�j
�@�@�V�O�T�@�@�g�����S�D�T�A�e���{�b�����O�D�Q�A�b���O�D�O�T�A�Q�D�O���m�����R�D�O�@�i�g�b�o�{�a�b�b�j
�i�P�S�|�T�|�U�j�@�b������
�@�@�v�A�l���̌ŗn�����ƒY�����̐͏o�d���A�x�őώ_�����A�^��n���i�U���n���j
�@�@�@�b���|�V�D�T�v�|�O�D�W�y���|�O�D�Q�s���|�O�D�P�b�|�O�D�P�T�x�@�i�b�Q�O�V�@�@�f�d�j�@
�@�@�@�b���|�V�D�P�l���|�Q�s���|�O�D�O�X�b�|�O�D�P�i�x�{�k���j�@�i�b�h�|�S�P�@�@�f�d�j
�@�@��������A�l���n�Y��
�@�@�@�b���|�U�l���n�|�O�D�T�s���@�iChrome-30�@�@�a�����������j
�@�@�@�b���|�R�l���n�|�Q�D�T�u�|�O�D�T�r���@�iChrome-90�@�@�a�����������j
�@�@�@�b���|�R�l���n�|�Q�D�T�u�|�P�r���|�O�D�T�s���|�Q�s���|�O�D�T�b�@�iChrome-90S�@�@�a�����������j
�@�@�b���|�Q�s���|�O�D�T�r���n
�@�@�@Alloy E�@�@�{�O�D�P�s��
�@�@�@Alloy H�@�@�{�O�D�T��y��
�@�@�@Alloy J�@
�@�@���V�A��
�@�@�@�b���|�O�D�P�T�s���|�O�D�Q�u�|�O�D�O�Q�b�@�i�a�w�|�Q�j
�i�P�S�|�T�|�V�j�@�u����
�@�@�u�|�S�b���|�S�s���i�{�x�j
�i�P�S�|�U�j�@��Z�_����
�@�@�P�̋����ł͂r���̗Z�_�Q�R�Q���A�����ł͂r���|�o���̋����g���U�R�D�O�r���|�R�V�D�O�o���̂P�W�R����
�@�ڈ��ƂȂ낤�B
�E�Q���n
�@�@��Ȓ�Z�_�Q��������Sn-�WZn�F�P�X�X���ASn-38Pb�F�P�W�R���i����Pb�͂j�ABi-42Sn�F�P�R�W���A
�@In-48Sn�F�P�P�V���AB��-�R�RIn�F�P�P�O���AIn-34Bi�F�V�Q���AGa-24.5In�F�P�T�D�V���ȂǁB
�@��Z�_�����ł悭�g�p�����̂͂a���A�o���A�r���A�b���A�y���A�h���ł���B
�@�h���͍����Ȃ̂œ��ɗZ�_��������p�r�Ɏg�p�A�܂��o���A�b���͓Ő������������悤�ɂȂ��Ă����B
�i�P�S�|�U�|�P�j�@�Z�����A�Z����fusible alloy
�@��Z�_�������Z�����A�Z����fusible alloy�Ə̂��邱�Ƃ�����B
�@��v�Ȃ��̂͋����ł��邪�A�����ł͂Ȃ��ʼnt�����i�ÌŁj�͈͂������̂�����B
�@��\�I�Ȃ��̂͂a���|�o���|�r���R���n�̃j���[�g���A���[�Y�A�_���Z�����⋌Cerro Metal Products��
�Z��������Z�����[Cerrolow�����ł���B
�@����Ȃ��̂ɂm���Ƃj�̍����m���j�i�i�b�N�A�V�V�m���|�Q�R�j�ŗZ�_�|�P�P���A���q�F��p�ށj������B
�@�@
�E�R���n
�@�퉷�t�̂�Ga-21.5In-16.0Sn�R�������͂P�O�D�V���AGa-21.5In-1�O.0Sn�i�K�����X�^���j�́|�P�X���Ƃ��B
�@
�@�a���|�o���|�r���n�@�@
| ������ | �a�� | �o�� | �r�� | �Z�_�� |
| �j���[�g��Newton | �T�O | �R�P | �P�X | �X�W |
| ���[�YRose | �T�O | �Q�W | �Q�Q | �X�T |
| �_���ZD'Arcet | �T�O | �Q�T | �Q�T | �X�T |
| �I�j�I��Onion | �T�O | �R�O | �Q�O | �X�Q |
| ���}���b�gMalotte | �S�U | �Q�O | �R�S | �X�U�|�P�Q�R |
�@

�@

�@�a���|�r���|�h���n
�@�@�t�C�[���hField�����F�T�P�h���|�R�Q�D�T�a���|�P�U�D�T�r���A�U�Q��
�@�@Cerrolow�P�V�S�F�T�V�a���|�P�V�r���|�Q�U�h���A�V�W�D�X��
�@

�@

�@�a���|�r���|�y���n
�@�@�R�������F�T�S�D�T�a���|�S�V�D�W�r���|�Q�D�V�y���@�P�R�O���@�i��������j
�@

�@�@
�@ �f���|�h���|�r���n
�@�@�@Indalloy�T�P�F�U�Q�D�T�f���|�Q�P�D�T�h���|�P�U�D�O�r���A�����P�O�D�V��
�@�@�@�K�����X�^���i�U�W�D�T�f���|�Q�P�D�T�h���|�P�O�r���j�́|�P�X���Ƃ������B
�@

�@�@
�@�f���|�r���|�y���n
�@�@�R�������_�F�P�V��
�@�@

�@���̂ق��f���|�h���|�y���R�������P�R���A�f���|�`���|�h���R�������P�S���ȂǁB
�E�����n
�@�@�a���|�o���|�r���|�b���n
| �a�� | �o�� | �r�� | �b�� | �Z�_�� | |
| �E�b�h���� | �T�O | �Q�T | �P�Q�D�T | �P�Q�D�T | �V�O |
| ���|���B�b�c���� | �T�O | �Q�V | �P�R | �P�O | �V�S |
�@�@�f���|�h���|�r���|�y���n
�@�@�@Indalloy�S�U�k�F�U�P�D�O�f���|�Q�T�D�O�h���|�P�R�D�O�r���|�P�D�O�y���A�U�D�T�|�V�D�U��
�@�@Cerro Alloys�Z������
�@�@�@�@Cerro Metal Products�i��Bolton Metal Products�j�̍����B
| �a�� | �o�� | �r�� | �b�� | �h�� | �r�� | �Z�_�� | |
| �a���|�o���|�r���{�b���A�r���n | |||||||
| Cerro SHIELD | �T�Q�D�T | �R�Q | �P�T�D�T�@ | �@ | �@ | �X�T | |
| Cerro SAFE | �S�Q�D�T | �R�V�D�V | �P�P�D�R | �W�D�T | �V�O�|�W�W | ||
| Cerro BENT | �T�O | �Q�U�D�V | �P�R�D�R | �P�O | �V�O | ||
| Cerromatrix | �S�W | �Q�W�D�T | �P�S�D�T | �X | �P�O�R�|�Q�Q�V | ||
| Cerrolow�V���[�Y �F�a���|�o���|�r���|�b���|�h���n | |||||||
| �P�P�V | �S�S�D�V | �Q�Q�D�U | �W�D�R | �T�D�R | �P�X�D�P | �S�V�D�Q | |
| �P�R�U | �S�X | �P�W | �P�Q | �Q�P | �T�W | ||
| �P�S�V | �S�W | �Q�T�D�U | �P�Q�D�W | �X�D�U | �S | �U�S�|�U�T | |
| �P�T�W | �T�O | �Q�U�D�V | �P�R�D�R | �P�O | �V�O | ||
�����x�q���[�Y�@
�@�@��ɂT�O�|�Q�O�O���t�߂����p����Ă���B
�i�P�S�|�T�|�Q�j�@�s���[�^�[pewter�@����߁i���ځA�n�N���E�j
�@Sn��̂̒�Z�_�����ŊȒP�ɒ����ł���B�H�|�p�����ޗ��B
�@���Sn���W�T�|�X�X����Cu�ASb�ABi�i�APb�E�E���͊����j�Ȃǂ�Y���B
�@�Z�_�͂P�V�O�|�Q�R�O���B
�i�P�S�|�U�|�R�j�@��������
�@�o���A�r���A�r�����Ȃ�B�r���͋ÌŖc�����N�������قȋ����B
�@�P�P���r�����R�O�A�R���r�����Q�O�A�Z�_�i�t�����j�͂Q�S�O�`�R�O�O���B
�i�P�S�|�U�|�S�j�@�o�r�b�g�E���^���i�z���C�g�E���^���j
�@Sn���听����Sb�ACu�A�iPb�j�A�o�����听���Ƃ�����̂�����B
�@�T���r�����P�R�A�R���b�����W�D�T
�@���낪�莲���Ƃ��ė��p�����B
�i�P�S�|�V�j�@�_�C�J�X�g����
�@�_�C�J�X�g�̂X�T���͂`�������Ŗ�S�����y�������Ƃ����B
�@�`�������ł͂قƂ�ǂ��`���|�r���|�b�������i�`�c�b�P�Q�A�ÌŊJ�n�T�W�O���j�ł���B
�@�y�������ł͂y���|�`���i�{�l�������j�i�y�c�b�Q�A�R�W�O���j�ł���B
�@�l�������ł͂l���|�`���|�y���|�l�������i�l�c�b�P�c�܂��͂`�y�X�P�c�A�U�O�O���j�ł���B
�@
| ���� | �Z�_�� | ��d | �M�`�����v�^���j |
| �y�� | �S�P�X | �V�D�P�S | �P�P�U |
| �l�� | �U�T�P | �P�D�V�S | �P�T�V |
| �`�� | �U�U�O | �Q�D�V�Q | �Q�R�U |
�E�_�C�J�X�g�p�`������
�@�@�`���|�r���n�i�`�c�b�P�j�A�`���|�r���|�l���n�i�`�c�b�R�j�A�`���|�l���n�i�`�c�b�T�j�A�`���|�r���|�b���n�i�`�c�b�P�O�A�P�Q�A�P�S�j�ȂǁB
�@�@�r���A�b���A�l���A�l���Ȃǂ̓Y���ŗZ�_�ቺ�A���x����A�ϐH�����P���s����B
�E�y������
�@�@�y���͘Z�����B�Z�����͈ٕ����̂��ߑY�����H������B
�@�@�y���|�`���|�b���n�i�y�c�b�P�j�A�y���|�`���n�i�y�c�b�Q�j�A�{�~�b�V�����^���n�ȂǁB
�@�@�o���A�b���A�r���͗��ԕ��H�̌����ƂȂ邽�ߌ����������B
�E�l������
�@�l���͘Z�����B
�@�_�C�J�X�g�p�͂i�h�r�ł�
�@�@�l�c�b�P�F�l���|�`���|�y���|�l��
�@�@�l�c�b�Q�F�l���|�`���|�l��
�@�@���ɂl���|�`���|�r���|�l���i�l�c�b�R�A�l�c�b�U�j
�@�����p�l�������̒��S�͂l���|�`���n�Ƃl���|�y���n�ł���B�ŗn�d���Ɛ͏o�d���i�����ԉ������j������B
�@�@�l���|�`���|�y���i�l�b�P�`�R�j�A�l���|�`���|�l���i�l�b�T�j
�@�y���Y������
�@�@�l���|�y���n��l���|�q�d�i��y�ށj�ɓY�������y���͌������������ʂ�L����B
�@�@�l���|�y���|�y���i�l�b�U�A�l�b�V�j�A�l���|�y���|�y���|�q�d�i�l�b�W�j�A�l���|�y���|�q�d�i�l�b�X�j�A
�@�l���|�y���|�y���|�q�d�i�l�b�P�O�j�B
�@���H
�@�@�e���A�m���A�b�������e�����y�ڂ��B
�@�`�r�s�l�K�i
�@�@�l�������ł͂킩��₷������`�r�s�l�K�i���悭���p�����A
�@�@����͂P���A�Q���ڂ���v�Y�����f�������A�R���A�S���ڂ̐��������ꂼ��̌��f�̗ʂ������A�T���ڂ�
�@�`�A�a�A�b�E�E�E�ŊJ������\���B
�@�@�`�y�c�X�P�c�͂`���X���A�y���P���������B
�@�@���f��
�@�@�`�F�`��
�@�@�b�F�b��
�@�@�d�F��y�ށi�~�b�V�����^���j
�@�@�g�F�s��
�@�@�j�F�y��
�@�@�k�F�k��
�@�@�l�F�l��
�@�@�p�F�`��
�@�@�r�F�r��
�@�@�x�F�v
�@�@�y�F�y��
�@�@�@�Ȃǂ������B
�@�@�_�C�J�X�g�p�͂`�y�n�A�`�l�n�A�`�r�n�A�`�d�n�ȂǁA�����p�͂`�y�n�A�d�y�n�A�p�d�n�A�y�d�n�A�v�d�n�ȂǁB
�@�@�W�L�p�͂`�y�n����ł���B
�i�P�S�|�W�j�@�M��������
�E�`������
�@�@�`���͏_�炩���̂ŁA�ŗn�����Ƃ`���|�b���̋K���������𗘗p����B
�@�@�`���|�`���|�b���n�R����Ԑ}�@�t����
�@�@

�@�@�@�`���|�`���|�b���R����Ԑ}�@�Q���̈�
�@�@�@

�@�@�@�@�@�@�`���|�b���F�K�����A�`���|�b���F����
�@�@�`���|�`���|�b���n�����̐F
�@�@�@

�@�@�@

�@�@�@
�@�@��X�Ȃ`�������̐F
�@�@�@�F�\�ʎ_�����̊��F
�@�@�@�@�`���|�Q�T�D�O�e���A�`���|�T�S�D�O�h��
�@�@�@��
�@�@�@�@�`���|�Q�O�`���@�@
�@�@�@�@�@�����ԉ������`���`���Q�@
�@�@�@�z���C�g�E�S�[���h�@�@�@�m���A�o���͋������𔒉�
�@�@�@�@�`���|�b���|�m���A�`���|�`���|�o��
�@�@�@�`���|�o���|�o���n
�@�@�@�@�@�`���|�o���F�Q������
�E�o���Ƃo��
�@�@�@�n�k�ł̑��ݗ��͂��Ƃ���
�@�@�@�`���@�V�T������
�@�@�@�o���@�P�T������
�@�@�@�o���@�@�T������
�@�@�@�`���@�@�S������
�@�@�@�n���@�P�D�T������
�@�@�@�q���A�h���A�q���@�P������
�@�@�@�q���@�@�O�D�V������
�@�@�Ƃ���A
�@�@�@�`���A�o���A�o�����n���A�q���A�h���A�q���A�q����荂���X���������B
�@�@�@�o����
�@�@�@�@�o���i�v���`�i�A�����j�A�h���i�C���W�E���j�j�A�n���i�I�X�~�E���j
�@�@�@�@�q���i���j�E���j�A�q���i���W�E���j�A�q���i���e�j�E���j
�@�@�o�������Ƃ��Ă�
�@�@�@�o���|�b��
�@�@�@�o���|�o���F�d���͏�����
�@�@�@�o���|�b��
�@�@�@�o���|�v
�@�@�@�o���|�o���|�b��
�@�@�@�o���|�q���A�o���|�h��
�@�@�@�@�q���A�h���F����������
�@�@�Ȃǂ�����A��ł͂o���̋�����
�@�@�@�o���|�X�T�O�i�X�T���o���j�F�q���A�b���A�b���A�v�A�h��
�@�@�@�o���|�X�O�O�F�o���A�b���A�q���A�h��
�@�@�@�o���|�W�T�O�F�o���A�b���A�q���A�h��
�@�����p�����B
�i�P�S�|�X�j�@���Y��
�@���Y���Ƃ͐����̂��Ƃ����邢�̓K���X�̂悤�ɂƏ̂����傫�ȐL�т����������ł���B
�@���鉷�x�ň��̘c���x�ň����������Ƃ��ɒ��Y���ł͋ψ�L�т��ȒP�ɂ͔j�f�Ɏ���Ȃ��B
�@�i�ʏ�̋����ł͂���ꏊ���炭�тꂪ�������j�f�Ɏ���B�j
�@���Y���ɂ͔����������Y���ƕϑԒ��Y��������B
�@�����������Y���͂P�O�ʂ��ȉ��̌��������������ɂ݂��A�������E�̂��ׂ�ƌ������̉�]�ɂ���Đ����A
�Q�������g�D�i�������邢�͋��́j�ł悭�݂��A�}��A��������A���J�j�J���E�A���C���O�A���H�M�����A�Č����Ȃǂɂ��
�����������s����B
�@�y���|�Q�Q�`���A�s�������iTi-6Al-4V�Ȃǁj�A�m��������A�Q���X�e�����X�ȂǁB
�@�ϑԒ��Y���͕ϑԓ_���㉺���鉷�x�T�C�N���Ő�����B
�i�P�S�|�P�O�j�@���U����
�@�������C�ɂ��U����������������̂Ō����@�\�ɂ��A�����^�A�������^�A�]�ʌ^�A�o���^������B
�@�@�����^�F���邢�͂���ȏ�̕��G�ȑg�D�A�����Đx���̂��鑊���ɓ�炩���������݂��������g�D�����B
�@�@�@�@�@�@�@�Џ����S�ȂǁB
�@�@�������^�F�T�C�����^���C�iFe-12Cr-3Al�j
�@�@�]�ʌ^�FMg����
�@�@�o���^�F�M�e���}���e���T�C�g�l���b������
�i�P�S�|�P�P�j�@�K���X��������
�@�K���X�Ƃ̐ڍ��A���ɋC�����~�ɃK���X�ƔM�c���������킹���������g�p�����B
�@KOVAR�R�o�[���@Fe-29Ni-17Co�@�@�M�c�����@��@�@�T�������i�P�O�|�U�^���j�@�@�@��]�_�K���X
�@�S�Q�A���C�@�@�@�@�@ Fe-42Ni�@�@�@�@�@�@�@�@�@�@�@�@�@��@�@�T������
�@�T�O�A���C�@�@�@�@�@ Fe-50Ni�@�@�@�@�@�@�@�@�@�@�@�@�@��@�P�O�������@�@�@�@�@�@�@�@�@�@�@�@�\�[�_���C���K���X
�@�S�U�V�A���C�@�@�@�@ Fe-47-6Cr �@�@�@�@�@�@�@�@�@�@�@��@�P�O������
�@�ȂǁB
�i�P�S�|�P�Q�j�@��M�c��������
�E�C���o�[�i�A���o�[�jInvar
�@��M�c���������B�L�����[�_�ȉ��̉��x�ł̎����̐ώ��c�ɂ��̐ϕω����i�q�U���ɂ��̐ϕω�
��ł������B
�@�@�C���o�[�@�@�@�@�@�@�@�@�@�@Fe-36Ni�@�@
�@�@�X�[�p�[�C���o�[�@�@�@�@Fe-32Ni-5Co�@�@
�@�@�X�e�����X�C���o�[�@�@�@Fe-54Co-9.5Cr
�@�@���ϐH���C���o�[�@Cr-Fe-Mn
�@�@�����x�C���o�[�@�@�@�@�@Fe-38Ni-Co-Ti
�@�@Fe-30Pt�AFe-30Pd
�E�G�����o�[Elinvar
�@�P�e���������B�����t�߂Ń����O���̉��x�W�����قƂ�ǃ[���ƂȂ�B
�@�ʏ�����E�����ł͉��x�㏸�ɂ��i�q�U���̔a���̂��ߔM�c�����A�����O���͒ቺ���邪�A
�@�G�����o�[�ł͋������̂ł̎��C�c���ʂɂ��A�����O���̉��x�ω����ŏ������B
�@�����O���͌����w�I�ٕ���������̂Ō������ʂȂǂ̑g�D����ɂ���Ă�������x�����ł���B
�@�@Fe-Ni�n
�@�@�@Elinvar�@�@�@�@Fe-36Ni-12Cr-(1�`2)Mn
�@�@�@Ni-span�@�@�@Fe-36Ni-9Cr
�@�@�@Iso-elastic�@Fe-36Ni -(7�`8)Cr-0.5Mo-0.6Mn
�@�@�@Metelinvar�@Fe-40Ni-6Cr-1.5Mo-2Mn
�@�@�@NiVarox�@�@�@Fe-36Ni-8Cr
�@�@Co�n
�@�@�@Coelinvar�@�@Co-Fe-Cr
�@�@�@Elcolloy�@�@�@Co-Fe-Cr-W-Ni
�i�P�S�|�P�R�j�@���f�z������
�@���f�z�������͐��f�Ɣ������������f�������`�����A���̔����͉t�I�Ő��f�̋z���E���o���\�ł���B
�@�z���͔��M�����ł����p�܂��͉������K�v�ŁA���o�͋z�M�����ʼn��M�܂��͌������K�v�ł���B
�@�������f�����͒P�̂ł͈��肩�ɂ߂ĕs���肩�����ꂩ�ƂȂ�A����Ȃ��̂͐��f����o���ɂ����A�s�����
���̂͐��f���z�����ɂ��������̗��҂�������������Ɛ��f�z�������Ƃ��Ďg�p���₷���Ȃ�B
�@���f�z�������͑����͋����ԉ������Ő��f�Ɛe�a���̂���`���f�Ɛe�a���̂Ȃ��a���f��
�`�a�i�s���e���j�A�`�a�Q�i�s���n���[�x�X�������j�A�`�Q�a�iMg2Ni�j�A�`�a�T�i�k���m���T�j�Ȃǂ̑g���̍�������ł���B
�@�i�s���n�a�b�b�ŗn�̌^����������j
�@�@�`�F�s���A�y���A�l���A��y�ތ��f�Ȃǁ@�a�F�e���A�m���A�b���Ȃ�
�@�l���͍�����v���i�R�O�O���j�A��y�ށA�s���n�͂P�O�O���O��Ŕ������s���B
�@���w���ł�LaNi5H6�AMgH2�ATiFeH2�������q����i�g�^�l�j�͂l�����Q��LaNi5�ATiFe���P�ł���B
�@�������f�����ɂ͋��������^�i�R�`����W�`���������f�j�A���L�����^�i�a�����f�j�A�C�I�������^�i�A���J���A�A���J���y�ށj
������A���f�z�������͎�ɋ��������^�i�l���n�̓C�I�������^�Ŕ����ɍ�����v���j�ł���B
�@���f�z�������ł͐��f�͌��q��ɂȂ���������̊i�q�Ԃ̂S�ʑ̈ʒu���邢�͂W�ʑ̈ʒu�ɐN�����ĐN���^���������`������B
�@���f�z�������͐��f�̋z���Ō����\���͕ω������̐ϖc�����N�����A���̂��ߔ����̌J��Ԃ��ɂ�����������B